Потенциальная функция - молекула
Cтраница 1
Потенциальная функция молекул GeIi3X ( симметрия C3f) содержит 12 элементов. [1]
Если потенциальная функция молекулы VN имеет п симметрически-эквивалентных минимумов без заметного проникновения локализованных волновых функций ( туннелирования) через барьеры между этими минимумами, то каждый уровень будет иметь n - кратное конфигурационное вырождение. Если имеется туннелирование сквозь барьеры, вырождение снимается, а это случается, когда высота барьера невелика по сравнению с колебательной энергией. В действительности всегда имеет место некоторое туннелирование, так как барьеры потенциальной энергии не являются бесконечно высокими, однако разрешение, достигаемое в эксперименте, часто не является достаточно высоким, чтобы заметить такое расщепление. Это имеет место и в случае метана. [2]
 |
Номенклатура силовых постоянных. [3] |
Процедура построения потенциальной функции молекулы набором указанных силовых постоянных не означает принятия какой-либо модели силового поля, она соответствует представлению функции разложением в ряд Тейлора и в этом смысле универсальна. [4]
Однако формулировка прямой задачи подразумевает наличие данных о потенциальной функции молекулы, а основным и в большинстве случаев единственным источником сведений о потенциальной функции являются значения частот нормальных колебаний. Тем самым возможности тех приложений теории колебательных спектров, которые требуют решения прямой задачи, ставятся в зависимость от успеха в решении обратной задачи, как принято называть задачу восстановления потенциальной функции по данным о ее колебательном спектре. В спектрохимических же исследованиях результаты решения обратной задачи - значения силовых постоянных - представляют непосредственный интерес, и именно их получение является обычно поводом к проведению теоретического расчета спектра. Силовые постоянные представляют собой параметры, характеризующие свойства электронной системы молекулы, причем характеристика эта дифференцирована по отдельным структурным элементам молекулы: связям, углам, группам атомов. Этим силовые постоянные выгодно отличаются от частот, характеризующих молекулу в целом, так как в общем случае частоты являются функциями одновременно всех силовых постоянных и кинематических параметров молекулы и могут непосредственно использоваться лишь при решении задачи идентификации вещества. Потенциальная энергия, фигурирующая в задаче о колебаниях ядер, является, вообще говоря, суммарной энергией электрон-ядерного, электрон-электронного и ядерно-ядерного взаимодействия и может быть определена при решении соответствующей квантовомеханической задачи. С этой точки зрения решение обратной колебательной задачи является экспериментальным определением той же величины, и полученные таким образом данные представляют важный резерв теории электронного строения молекул. [5]
Обратная колебательная зедача ( ОКЗ) - определение потенциальной функции молекулы по данным из колебательных спектров - имеет единственное решение в простейших случаях, характеризуемых вековыми уравнениями не выше третьей степени, и при условии, что наряду с частотами колебаний можно использовать данные о величинах постоянных колебательно-вращательного взаимодействия или среднеквадратичных амплитудах колебаний. Обсуждены проблемы применения теории колебательных спектров молекул в тех случаях, когда нет оснований рассчитывать на получение единственного решения ОКЗ; рассмотрены методы исследования множества решений. Приведена сводка силовых постоянных простейших неорганических молекул, потенциальные функции которых определены однозначно. [6]
Для больших значений у поперечное сечение потенциальной поверхности приближается к потенциальной функции молекулы Н2 в основном состоянии. [7]
Теорема Борна-Оппенгеймера ничего не говорит нам о том, какой должна быть потенциальная функция молекулы. Важно только, чтобы она была непрерывной функцией координат ядер. Поэтому с точки зрения квантовой механики все три пути одинаково правомерны. [8]
Указанный путь при формулировке задачи в естественных координатах приводит к введению в потенциальную функцию молекулы членов вида a. Такой метод позволяет приближенно учесть неточность основных диагональных коэффициентов взаимодействия путем введения очень ограниченного числа малых констант. По идее, этот шаг эквивалентен нулевому приближению расчетной схемы, в которой учитывались только диагональные коэффициенты взаимодействия. Несмотря на грубо приближенный характер такого учета ангармоничности, можно думать, что он является все же разумным и, более того, обязательным шагом в решении этой сложной проблемы. [9]
Теорема Борна - Оппенгеймера ничего не говорит о том, какой должна быть потенциальная функция молекулы. Важно только, чтобы она была непрерывной функцией координат ядер. Поэтому с точки зрения квантовой механики все три пути одинаково правомерны. [10]
С другой стороны, результаты CAB могут быть использованы в обратной спектроскопической задаче для восстановления структуры и потенциальной функции молекулы, исходя из известных экспериментальных значений СП. Преимущество аналитического представления соотношений для СП в обратной задаче состоит в том, что в CAB соотношения липа (1.27) достаточно получить только раз. После этого итерационные циклы методов минимизации содержат подстановку численных значений МП в (1.27), которая требует минимальных затрат машинного времени. При чисто численном способе расчетам каждой итерации должна заново повторяться процедура решения уравнения Шрединг ера методами возмущений, что делает задачу восстановления потенциала трудно реализуемой. [11]
Частные случаи адсорбции ( локализованная, нелокализованная адсорбция) должны вытекать из общей статистической теории, которая базируется только на зависимости потенциальной функции V молекул адсорбата вблизи поверхности от всех координат. Степень заторможенности тех или иных движений молекул адсорбата определяется этой функцией V и температурой. Были получены общие статистические выражения для одно-компонентного [2, 10-18], двукомпонентного [19] и многокомпонентного 120 ] адсорбированного газа, аналогичные вириальным уравнениям для реального газа. [12]
Эти группы полезны при изучении, например, активных в ИК - и КР-спектрах основных колебаний, для нахождения отличных от нуля членов в потенциальных функциях молекул и для выбора атомных орбитальных волновых функций, которые могут участвовать в образовании конкретных молекулярных орбиталей. Хотя точечные группы молекул вводятся и определяются в гл. [13]
Для подсчета энергий ( энтальпий) изомеризации нет необходимости находить энтальпии атомизации, суммируя энтальпии связей, - достаточно лишь сравнить энергии напряжения, которые были получены минимизацией потенциальных функций молекул. [14]
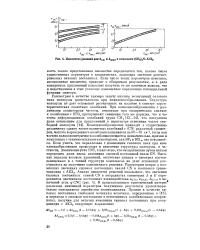 |
Множество решений для fcCN и ACNC в комплексе ( CH3 3NA1G1. [15] |
Страницы: 1 2