Потенциальная функция - межмолекулярное взаимодействие
Cтраница 2
В качестве характеристических параметров при обобщении коэффициентов переноса чистых жидкостей обычно используются критические параметры, значения коэффициентов, им соответствующие, или параметры потенциальной функции межмолекулярного взаимодействия, т.е. те параметры, которые имеют четкий физический смысл и могут быть достаточно точно определены экспериментально или расчетным путем. [16]
Характеризуется он такими параметрами, как межмолекулярные расстояния, а для молекул, не обладающих сферической симметрией, также и значениями координатных углов, задающих взаимную ориентацию. Силовой аспект связан с потенциальной функцией межмолекулярного взаимодействия и отражает энергетическую неравноценность различных молекулярных построений. [17]
VI-XI) термодинамические характеристики адсорбционного равновесия рассмотрены молекулярно-статистическим методом на основе соответствующих потенциальных функций межмолекулярного взаимодействия адсорбат - адсорбент и адсорбат - адсорбат. [18]
Таким образом, теоретическое исследование связи таких чувствительных характеристик веществ, как индексы удерживания, со структурой молекул представляет принципиальный интерес для исследования общей проблемы межмолекулярных взаимодействий. По мере уточнения экспериментальных значений VA, i и /, с одной стороны, и уточнения зависимости потенциальных функций межмолекулярного взаимодействия от их формы и параметров ( см. [12]) - с другой, можно будет, по-видимому, установить зависимость параметров атом-атомных потенциальных функций, например функций фс с и Фс н от таких факторов, как характер окружения данного атома С в молекуле ( атомами С и Н в случае углеводородов), от характера и степени напряженности циклов и от электронной конфигурации атомов - наличия кратных связей, сопряжения, конденсации циклов и др. Эти полуэмпирические зависимости, найденные с использованием газохроматографического метода, представляют также интересный объект для исследования методами квантовой химии. [19]
В задачу этой теории входит молеку-лярно-статистический расчет изотерм адсорбции ( константравновесия, вириальных коэффициентов, удерживаемых объемов при нулевых, малых и средних заполнениях поверхности, а также других термодинамических величин), теплот и энтропии адсорбции, теплоемкости адсорбционных систем. Конфигурационные интегралы, входящие в статистические выражения этих термодинамических величин, можно вычислить, на основе полуэмпирических выражений для потенциальных функций межмолекулярного взаимодействия адсорбат - адсорбент и адсорбат-адсорбат. [20]
Из предыдущих разделов этой главы видно, что проделанная за последние годы работа по приготовлению новых кристаллических непористых адсорбентов с близкой к однородной поверхностью, пористых кристаллов и чистых молекулярноситовых углей, макропористых полимерных неорганических, органических и смешанных ( неорганических с органическим модифицирующим слоем) адсорбентов с различными функциональными группами позволила значительно расширить диапазон селективности адсорбентов и емкости адсорбционных колонн. Параллельно разрабатывалась также и лежащая в основе селективности разделения молекулярная теория адсорбции на близких к однородным адсорбентах, в основном в направлении создания метода количественных молекулярно-статистических расчетов и предсказания термодинамических характеристик удерживания многих молекул при использовании атом-атомного приближения для потенциальных функций межмолекулярного взаимодействия молекул с адсорбентом. [21]
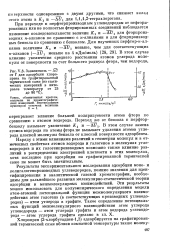 |
Зависимость - ДС7 от Г для адсорбции хлоро-прена на графитированной термической саже ( из статических измерений в интервале температур от 25 до 80 С. [22] |
Результаты экспериментального исследования адсорбции моно - и полигалогенпроизводных углеводородов, помимо значения для идентифицирования в аналитической газовой хроматографии, необходимы для дальнейшего развития молекулярно-статистическои теории адсорбции и межмолекулярных взаимодействий. Такое определение потенциальных функций межмолекулярного взаимодействия атом углерода углеводорода - атом углерода графита и атом водорода углеводорода - атом углерода графита сделано в гл. [23]
Другой путь нахождения уравнения состояния адсорбированного вещества, уравнения изотермы адсорбции и зависимостей АС / и АС от Г представляет использование некоторых приближенных моделей для адсорбированного вещества. III) связь входящих в эти уравнения констант с потенциальными функциями межмолекулярного взаимодействия адсорбат - адсорбент и адсорбат - адсорбат не раскрывается. Эти константы определяются из опытных данных. Такое описание термодинамических свойств адсорбционной системы во многих случаях, особенно при достаточно высоких заполнениях поверхности, оказывается единственно возможным. Вместе с тем обработка экспериментальных данных с помощью таких уравнений позволяет найти константы, отражающие межмолекулярные взаимодейтвия адсорбат - адсорбент [ константу Генри K. III) ] и адсорбат - адсорбат и исследовать их зависимость от природы адсорбата и адсорбента и температуры. [24]
Решение задачи оптимизации использования молекулярных взаимодействий компонентов смеси путем выбора соответствующей неподвижной фазы ( адсорбента или жидкости, молекулярного сита) может быть найдено лишь на основе теории межмолекулярпых взаимодействий в газах и жидкостях и между газами и жидкостями и твердым адсорбентом. Эта теория основывается на результатах изучения геометрии и химической природы молекул газа, молекул жидкости и поверхности твердого тела. Она представляет собою молекулярную теорию, поскольку ее задачей в области хроматографии является объяснение связи с молекулярными параметрами и вычисление термодинамических констант адсорбционного или распределительного равновесия ( например, констант Генри для нулевых проб), определяющих селективность. Отсюда ясно значение молекулярно-стати-стических расчетов для развития молекулярных теорий адсорбции или растворения и их приложений к хроматографии, поскольку именно статистическая термодинамика указывает правильную количественную связь констант термодинамического равновесия с потенциальными функциями межмолекулярного взаимодействия. Однако по мере усложнения адсорбционной системы использование статистической термодинамики для количественных расчетов удерживаемых объемов встречает затруднения, особенно в случае специфических взаимодействий и неоднородных поверхностей. Вместе с тем увеличение энергии и характеристичности взаимодействия влечет за собой возможность получения новой важной информации о специфическом молекулярном взаимодействии при использовании комплекса спектроскопических методов. Это помогает наполнить даваемые хроматографическими и термодинамическими исследованиями полуэмпирические и феноменологические связи между различными параметрами эвристическим содержанием в смысле возможного приближения к молекулярным основам взаимодействия и селективности. Сюда относится, в частности, использование регулирования специфических взаимодействий, в частности электростатических взаимодействий диполышх и квад-рупольных молекул с поверхностями ионных кристаллов и с поверх-постными функциональными группами, использование и регулирование водородной связи и вообще взаимодействий донорно-акцепторного типа и процессов комплексообразования. [25]
Решение задачи оптимизации использования молекулярных взаимодействий компонентов смеси путем выбора соответствующей неподвижной фазы ( адсорбента или жидкости, молекулярного сита) может быть найдено лишь на основе теории межмолекулярных взаимодействий в газах и жидкостях и между газами и жидкостями и твердым адсорбентом. Эта теория основывается на результатах изучения геометрии и химической природы молекул газа, молекул жидкости и поверхности твердого тела. Она представляет собою молекулярную теорию, поскольку ее задачей в области хроматографии является объяснение связи с молекулярными параметрами и вычисление термодинамических констант адсорбционного или распределительного равновесия ( например, констант Генри для нулевых проб) г определяющих селективность. Отсюда ясно значение молекулярно-стати-стических расчетов для развития молекулярных теорий адсорбции или растворения и их приложений к хроматографии, поскольку именно статистическая термодинамика указывает правильную количественную связь констант термодинамического равновесия с потенциальными функциями межмолекулярного взаимодействия. Однако по мере усложнения адсорбционной системы использование статистической термодинамики для количественных расчетов удерживаемых объемов встречает затруднения, особенно в случае специфических взаимодействий и неоднородных поверхностей. Вместе с тем увеличение энергии и характеристичности взаимодействия влечет за собой возможность получения новой важной информации о специфическом молекулярном взаимодействии при использовании комплекса спектроскопических методов. Это помогает наполнить даваемые хроматографическими и термодинамическими исследованиями полуэмпирические и феноменологические связи между различными параметрами эвристическим содержанием в смысле возможного приближения к молекулярным основам взаимодействия и селективности. Сюда относится, в частности, использование регулирования специфических взаимодействий, в частности электростатических взаимодействий дипольных и квад-рупольных молекул с поверхностями ионных кристаллов и с поверхностными функциональными группами, использование и регулирование водородной связи и вообще взаимодействий донорно-акцепторного типа и процессов комплексообразования. [26]
Последний способ определения параметров, как и предыдущий, позволяет оценить параметры потенциалов Ф независимым от экспериментальных адсорбционных данных путем. Такой способ оценки Ф сравнительно легко применим к любым системам адсорбат - адсорбент. Оцененные этим способом значения потенциальной энергии Ф в минимуме обычно получаются близкими к опытным значениям теплот адсорбции. Однако функции Ф, полученные этим способом, недостаточно точны для проведения более глубоких исследований термодинамических свойств разных адсорбционных систем. Для получения более точных потенциальных функций межмолекулярного взаимодействия простых и сложных молекул с адсорбентом необходимо использовать экспериментальные адсорбционные данные. В работах Киселева, Пошкуса и Афреймовича [12, 13, 136-139] был применен этот способ расчета и предложен простой способ уточнения главного параметра сил притяжения путем использования экспериментальных значений константы Генри Kit определенных при разных температурах. [27]
Если же система неравновесная и существуют градиенты, то функция распределения определяется из интегро-дифференциального уравнения Больцмана. Уравнение Больцмана для случая, мало отличающегося от равновесного, когда потоки линейны по отношению к производным, может быть решено с помощью метода теории возмущений, развитого Чепменом и Энскогом. Таким образом, рассматриваются лишь парные столкновения. В то же время длина свободного пробега молекулы должна быть мала по сравнению с макроскопическими размерами, чтобы газ можно было рассматривать как сплошную среду. В этом случае из уравнения Больцмана получаются гидродинамические уравнения Навье-Стокса и выражения для векторов потоков. Коэффициенты переноса определяются векторами потоков и выражаются через интегралы Q s [30], значение которых зависит от вида потенциальной функции межмолекулярного взаимодействия. [28]
Вместе с тем, вириальные выражения имеют и определенные ограничения. Во-первых, экспериментальное определение и теоретический расчет коэффициентов более высоких членов вири-ального разложения изотермы адсорбции встречают большие трудности. В этом приближении все изменения термодинамических свойств адсорбата и адсорбента при адсорбции приписываются адсорбату. Твердое тело в этом приближении рассматривается только как источник внешнего потенциального поля, постоянного во времени и не зависящего от температуры, давления и адсорбции. Это допущение, по-видимому, справедливо для многочисленных практически важных случаев адсорбции на нелетучих, нерастворяющих адсорбат адсорбентах. Кроме того, вириальные разложения справедливы и для неинертного твердого тела. Однако в последнем случае коэффициенты вириальных разложений определяются соответствующими потенциальными функциями межмолекулярного взаимодействия, усредненными по всем возможным конфигурациям адсорбента при заданных его химическом потенциале и температуре. [29]
Если в газе отсутствуют градиенты скор ости, температуры и концентрации, то функция / ( г, С [, т) представляет собой распределение Максвелла. Если же система неравновесная и существуют градиенты, то функция распределения определяется из интегро-дифференциального уравнения Больцмана. Уравнение Больцмана для случая, мало отличающегося от равновесного, когда потоки линейны по отношению к производным, может быть решено с помощью метода теории возмущений, развитого Чепменом и Энскогом. Уравнение Больцмана справедливо лишь для достаточно малых плотностей газа, когда влиянием столкновений более чем двух молекул можно пренебречь. Таким образом, рассматриваются лишь парные столкновения. В то же время длина свободного пробега молекулы должна быть достаточно мала, чтобы газ можно. В этом случае из уравнения Больцмана получают гидродинамические уравнения Навье-Стокса и выражения для векторов потоков. Коэффициенты переноса определяются векторами потоков и выражаются через интегралы Q ( s [12], значение которых зависит от вида потенциальной функции межмолекулярного взаимодействия. [30]
Страницы: 1 2