Диссоциация - йодистый водород
Cтраница 1
Диссоциация йодистого водорода подробно изучена Готфейлем и потом Лемуаном, из исследований котэрзго извлекаем следующие сведения. Разложение HJ явно при 180, но идет медленно, с повышением температуры скорость и предел разложения возрастают. Corenwinder), которая ускоряет также и распадение HJ, но я само пэ себе, но только медленно. Предел обратимэй реакции остается тот же с губчатою платиною или без нее. Увеличение давления очень сильно ускоряет ход реакции образования HJ, а потому губчатая платина, сгущая газы, действует подобно давлению. При атмосферном давлении распадение HJ достигает предела при 250 в несколько месяцев, а при 440 в несколько часзв. Если же давление, под которым 2HJ переходит в Н2 - f - J2, будет 4 / ч атм, то предел 24 %, под давлением Ч, атм. [1]
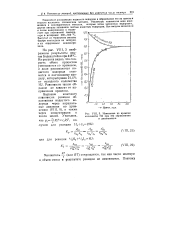 |
Изменение во времени. [2] |
Равновесие диссоциации йодистого водорода и образования его из просты х веществ изучалось статическим методом. [3]
Вследствие этого степень диссоциации йодистого водорода при данной температуре остается постоянной, несмотря на то, что давление может увеличиваться в несколько раз. [4]
Такая константа равновесия называется константой диссоциации йодистого водорода на элементы. [5]
Это уравнение и выражает зависимость степени диссоциации йодистого водорода от температуры. [6]
Рассмотрим приложение закона действующих масс к обратимой реакции диссоциации йодистого водорода. [7]
Для реакции диссоциации йодистого водорода HI HI - Н2 12 экспериментально найденная энергия активации составляет 45 900 кал. [8]
 |
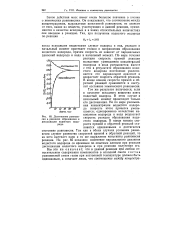
Простой прибор для превращения легко конденсирующихся газов в жидкое состояние путем охлаждения. [9] |
Реакция иода с водородом в гомогенной газообразной фазе протекает по механизму бимолекулярных реакций ( стр. Скорость реакции при 300 мала, и реакция не идет до конца ( степень диссоциации йодистого водорода при этой температуре составляет примерно 19 %); при более высокой температуре степень диссоциации еще выше. Поэтому с помощью данного метода нельзя получить чистый HI, не содержащий свободного иода. [10]
Так как в обоих случаях условием равновесия служит равенство скоростей прямой и обратной реакций, то из него вытекает одно и то же выражение константы равновесия реакции. На рис. 85 показано изменение парциального давления йодистого водорода со временем по опытным данным при реакции диссоциации йодистого водорода и при реакции получения его. [11]
 |
Достижение равнове - скорость реакции образования йодистого водорода. В конце концов скорости прямой и обратной реакций становятся одинаковыми и достигается. [12] |
Так как в обоих случаях условием равновесия служит равенство скоростей прямой и обратной реакций, то из него вытекает одно и то же - выражение константы равновесия реакции. На рис. 85 показано изменение парциального давления йодистого водорода со временем по опытным данным при реакции диссоциации йодистого водорода и при реакции получения его. [13]
Если в процессе обратимой химической реакции общее число молекул не меняется, изменение давления не влияет на состояние химического равновесия системы. Так, например, реакция, протекающая по уравнению Н2 I2 2HI, не сопровождается изменением общего числа молекул в системе. Вследствие этого степень диссоциации йодистого водорода при данной температуре остается постоянной, несмотря на то что давление может увеличиваться в несколько раз. [14]
Независимыми называются те компоненты системы, содержание которых не зависит от содержания других компонент. Независимые компоненты не могут превращаться друг в друга никакой реакцией, происходящей в системе. Например, в случае диссоциации йодистого водорода ( 2HJ Н2 J2) независимых компонент две: Н2 и J2, HJ является зависимой компонентой. Исключить массу HJ из термодинамического потенциала можно лишь после того, когда решена задача равновесия. Большая часть дополнительных условий между виртуальными изменениями 8УИ дается в вариационной форме, и часто не существует практической возможности исключить зависимые массы Л1, если не решить задачу до конца. [15]
Страницы: 1 2