Диссоциация - гидроокись - аммоний
Cтраница 1
Диссоциация гидроокиси аммония ( NH4OH) незначительна, поэтому при проведении вычислений ею можно пренебречь. [1]
Диссоциация гидроокиси аммония ( NH4OH) незначительна, поэтому ею можно пренебречь. [2]
Диссоциация гидроокиси аммония уменьшается в присутствии его солей. Поэтому не осаждается гидроокись магния. [3]
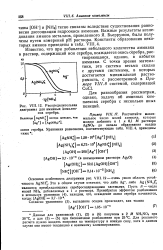 |
Распределительная диаграмма для аминных комплексов серебра. [4] |
ОН ] и [ NH ] тесно связаны вследствие существования равновесия диссоциации гидроокиси аммония. [5]
Выше ионное равновесие сместится влево - в сторону молекулиза-ции, и степень диссоциации гидроокиси аммония уменьшится. [6]
Раствор ( NH4) 2S слабощелочной ( рН 9 3), так как константа диссоциации сероводорода в 200 раз меньше, чем константа диссоциации гидроокиси аммония. [7]
Единственное широко распространенное слабое основание - гидроокись аммония. Константа диссоциации гидроокиси аммония имеет величину 1 8ЫО - Б при 25 С. [8]
Концентрация катиона NH4 слагается из концентрации катионов основания и соли. По степень диссоциации гидроокиси аммония весьма мала, а в присутствии соли, имеющей одноименный катион МНд, она еще больше снижается. [9]
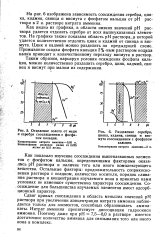 |
Отделение золота от меди и серебра соосаждением с фосфатом кальция.| Разделение серебра, цинка, кадмия, свинца и висмута соосаждением с фосфатом кальция. [10] |
Сдвиг кривых соосаждения в область меньших значений рН раствора при увеличении концентрации нитрата аммония наблюдается только для элементов, способных образовывать аммиакаты. Нитрат аммония препятствует диссоциации гидроокиси аммония. Поэтому даже при рН 7 5 - 8 0 в растворе имеется достаточное количество аммиака для связывания того или иного иона в комплекс. [11]
В 250 мл воды растворено 2 г аммиака. Вычислить активность ионов ОН - и степень диссоциации гидроокиси аммония в полученном растворе и при разбавлении его в 10, в 100 и в 1000 раз. [12]
В 250 мл воды растворено 2 г аммиака. Вычислить ак-цвность ионов ОН - и степень диссоциации гидроокиси аммония в полученном растворе и при разбавлении его в 10, в 100 и в 1000 раз. [13]
Для осаждения гидроокиси алюминия используют обычно раствор аммиака. Но, несмотря на относительно небольшое значение константы диссоциации гидроокиси аммония ( 1 8 - 10 - 5), все же и в этом случае очень легко недоосадить алюминий вследствие частичного растворения алюминия в избытке аммиака. Для того чтобы понизить рН раствора, следует воспользоваться буферным раствором ( см. стр. [14]
Однако неправильно, как это неоднократно делали раньше, считать ее за константу диссоциации гидроокиси аммония. [15]
Страницы: 1 2