Ступенчатая диссоциация
Cтраница 3
В реальных растворах имеет место ступенчатая диссоциация. В растворах комплексных соединений присутствуют все комплексы данного соединения, находящиеся в химическом равновесии. [31]
Какие электролиты подвергаются в растворах ступенчатой диссоциации. [32]
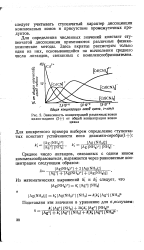 |
Зависимость концентраций различных ионов. [33] |
Для определения численных значений констант ступенчатой диссоциации применяются различные физико-химические методы. Здесь вкратце рассмотрим только один из них, основывающийся на вычислении среднего числа лигандов, связанных с комплексообразователем. [34]
Следует отметить, что при ступенчатой диссоциации всегда наиболее легко протекает первая ступень, так как незаряженная молекула легче диссоциирует, чем ион. [35]
Переходы окраски его связаны со ступенчатой диссоциацией и образованием анионов различного состава. При рН 1 - 7 образуются двухзарядные анионы, окрашенные в желтый цвет, при рН 7 4 - 10 в растворе находятся трехзарядные анионы фиолетового цвета, а при рН выше 10 - четырехзарядные анионы синего цвета. [36]
Вследствие этого в ряде случаев наблюдается ступенчатая диссоциация, вызывающая появление двух скачков титрования на потенциометричеекой кривой или двух изломов на кондуктомет-рической. [37]
В водном растворе фосфорная кислота подвергается ступенчатой диссоциации ( с. Будучи трехосновной кислотой, она образует соли - фосфаты - трех видов: 1) фосфаты - замещены все атомы водорода в фосфорной кислоте, например К3РО4 - фосфат калия, ( NHJsPC - фосфат аммония; 2) гидрофосфаты - замещены два атома водорода, например К2НРО4 - гидрофосфат калия, ( МН4) 2НРС4 - гидрофосфат аммония; 3) ди-гидрофосфаты - замещен один атом водорода, например КН2РО4 - дигидрофосфат калия; NH4H2PO4 - дигидрофосфат аммония. [38]
В водном растворе фосфорная кислота подвергается ступенчатой диссоциации. [39]
В водном растворе фосфорная кислота подвергается ступенчатой диссоциации ( с. Будучи трехосновной кислотой, она образует соли - фосфаты - трех видов: 1) фосфаты - замещены все атомы водорода в фосфорной кислоте, например К3РО4 - фосфат калия, ( NH4) 3PO4 - ф сФат аммония; 2) гидрофосфаты - замещены два атома водорода, например К2НРО4 - гидрофосфат калия, ( NH4) 2HPO4 - гидрофосфат аммония; 3) ди-гидрофосфаты - замещен один атом водорода, например КН2РО4 - дигидрофосфат калия; NH4H2PO4 - дигидрофосфат аммония. [40]
В водном растворе фосфорная кислота подвергается ступенчатой диссоциации. [41]
Однако строение анионов, образующихся при ступенчатой диссоциации протонов из кислоты, не исследовано, хотя это весьма важно для правильного понимания механизма комп-лексообразования ОЭДФК. [42]
Для многоосновных кислот и многокислотных оснований характерна ступенчатая диссоциация с отрывом одного иона Н или ОН - по каждой ступени. Таким образом, число ступеней определяется основностью кислоты или кислотностью основания. Поскольку первый ион отрывается от нейтральной частицы, а последующие от частиц с зарядом противоположного знака, который увеличивается с каждой ступенью на единицу, то степень электролитической диссоциации сильно уменьшается при переходе от первой ступени к каждой следующей. [43]
В связи с особенностью многоосновных кислот подвергаться ступенчатой диссоциации находится их способность образовывать кислые соли; например: KHSO4 - кислый сернокислый калий. [44]
Страницы: 1 2 3