Вольфрамат
Cтраница 1
Помимо вольфраматов, известны галоидные соли вольфрама. [1]
Большинство вольфраматов мало растворимо в воде. Вводя в раствор соль железа ( III) и осаждая последнее аммиаком, можно количественно выделить в осадок и следы вольфрама. [2]
Осадки вольфраматов адсорбируют трудно отделяемые соли других кислот или образуют с ними двойные соли и гетеро-полисоединения. Поливалентные металлы ( железо, марганец, висмут и др.) могут осаждаться в виде вольфрамата металлов смешанной валентности. Большинство вольфраматов указанных металлов образует ряд кристаллогидратов. Степень гидратации, а также образование того или иного изополи - и гетерополисоединения зависят и кислотности раствора. [3]
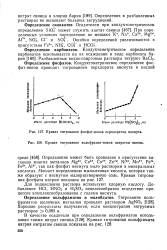 |
Кривая титрования фосфат-ионов перхлоратом висмута.| Кривая титрования вольфрамат-ионов нитратом свинца. [4] |
Определение вольфраматов и молибдатов. [5]
 |
Решетка вольфрамата кальция. CaW04. [6] |
Свечение вольфраматов возбуждается под действием корпускулярных лучей: а, р и электронов в разрядных трубках. Для возбуждения могут применяться также ультрафиолетовые лучи среднего и коротковолнового диапазона. [7]
Синтез вольфраматов и молибдатов с целью получения новых материалов для радиоэлектроники. [8]
Большинство вольфраматов мало растворимо в воде. Вводя в раствор соль железа ( III) и осаждая последнее аммиаком, можно количественно выделить в осадок и следы вольфрама. [9]
Монокристаллы вольфраматов щелочноземельных элементов, содержащие небольшие примеси парамагнитных ионов трехвалентных элементов, представляют интерес для квантовой физики. Экспериментальные данные, полученные Крюковой, позволяют сделать практические рекомендации. Введение редкоземельных элементов в кристаллы исследованных вольфраматов следует проводить в расплавах хлористого лития, а очистку их от нежелательных примесей редкоземельных элементов в расплавах хлоридов натрия и калия при возможно низкой температуре. [10]
Способность вольфраматов щелочных металлов растворять кремниевую кислоту с образованием кремневольфрамовой кислоты H4 [ Si ( W3O10) 4 ] 2H2O, которая, в свою очередь, может растворять некоторые соединения железа, марганца и кальция, сыграла большую роль в образовании вольфрамовых месторождений и миграции вольфрама и других элементов в природе. [11]
Синтез вольфраматов щелочноземельных металлов необходимо проводить путем двухкратного обжига смеси заданного состава с промежуточным перетиранием спека и дошихтовкой последнего трехоки-сью вольфрама. Оптимальная температура синтеза лежит в пределах от 850 до 900 С. Продолжительность каждой выдержки при температуре синтеза равна 1 - 2 час. [12]
Получается разложением вольфраматов НС1 или HNOa и последующим1 прокаливанием выделившейся вольфрамовой кислоты. [13]
Получается разложением вольфраматов ( солей вольфрамовой кислоты) НС1 и НМО3 с последующим прокаливанием выделившейся вольфрамовой кислоты. [14]
Получается разложением вольфраматов ( солей вольфрамовой кислоты) НС1 и HNO3 с последующим прокаливанием выделившейся вольфрамовой кислоты. [15]
Страницы: 1 2 3 4