Конкурентное ингибирование
Cтраница 1
 |
Необратимое ингибирование SH-фермента иодацетамидом. [1] |
Конкурентное ингибирование можно количественно изучать на основе теории Михаэлиса-Ментен. [2]
Конкурентное ингибирование проще всего можно распознать экспериментальным путем, определив влияние концентрации ингибитора на зависимость начальной скорости реакции от концентрации субстрата. Для выяснения вопроса о том, по какому типу-конкурентному или неконкурентному-происходит обратимое ингибирование фермента ( дополнение 9 - 3), весьма удобно преобразовать уравнение Михаэлиса-Ментен в линейную форму. Чаще всего для этой цели используют метод двойных обратных величин. [4]
Конкурентное ингибирование имеет место в тех случаях, когда какое-либо вещество, присутствующее в концентрации, во много раз превосходящей концентрацию фермента, способно вступать в обратимую реакцию с ферментом и образовывать с ним промежуточный комплекс фермент - ингибитор, при распаде которого продукты реакции не образуются. [5]
Конкурентное ингибирование может быть вызвано веществами, имеющими структуру, похожую на структуру субстрата, но несколько отличающуюся от структуры истинного субстрата. [6]
Конкурентное ингибирование - тип ингибирования фермента, которое можно снять, повысив концентрацию субстрата. [7]
Явление конкурентного ингибирования, которое наблюдается в гетерогенном катализе, можно также рассмотреть на примере ферментативного катализа. Предполагается, что ингибитор S сильно сорбируется на тех же самых активных местах Е, что и субстрат S, и, таким образом, замедляет реакцию за счет понижения активных мест. [8]
 |
Необратимое ингибирование фермента иодуксусной кислотой. Иод вступает в реакцию с сульфгидрильными группами фермента. [9] |
Явление конкурентного ингибирования помогает понять механизм действия некоторых лекарственных препаратов, в частности сульфаниламидов. [10]
Эта простая схема конкурентного ингибирования (4.20) формально остается справедливой также и при высоких концентрациях субстрата. Но в этом случае в результате изменения среды возрастает растворимость ингибитора в водном растворе, что термодинамически затрудняет его экстракцию активным центром фермента. Фактически на опыте с увеличением концентрации субстрата возрастает эффективное значение константы KI диссоциации фермент-ингибиторного комплекса, что и приводит к увеличению скорости процесса ( ср. [11]
Далее, даже при чисто конкурентном ингибировании продуктами идеальная точка пересечения на оси ординат практически не наблюдается вследствие определенных экспериментальных погрешностей и не может служить достоверным критерием ингибирования продуктами. Наконец, S-образные отклонения от прямолинейной зависимости на рис. 3 при деградации олигомеров наблюдаются лишь на начальных и на завершающих участках полной кинетической кривой ( соответственно при степенях конверсии в мономер менее 10 % и более 80 % для обсуждаемого случая гидролиза мальтодекстринов), которые редко анализируются на практике и обычно не считаются достоверными. [12]
При добавлении органических субстратов происходит конкурентное ингибирование, которое является следствием конкурентного связывания в полости циклоамилозы. [13]
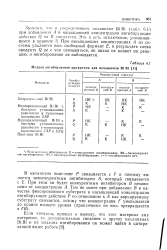 |
Модели ингибирования продуктом для механизмов Bi Bi [ И ]. [14] |
Используемые обозначения: К - конкурентное ингибирование, БК - бесконкурент ное ингибирования. КК - неконкурентное ингибироваиие, ( -) - ингибирования нет. [15]
Страницы: 1 2 3 4
