Неконкурентное ингибирование
Cтраница 1
Неконкурентное ингибирование - тип ингибирования ферментов, которое не снимается при повышении концентрации субстрата. [1]
Неконкурентное ингибирование, при к-ром И. [2]
 |
Действие конкурентного ингибитора ( схема по В.Л. Кретовичу. [3] |
Неконкурентное ингибирование вызывается веществами, не имеющими структурного сходства с субстратами и часто связывающимися не с активным центром, а в другом месте молекулы фермента. Степень торможения во многих случаях определяется продолжительностью действия ингибитора на фермент. При данном типе ингибирования благодаря образованию стабильной ковалентной связи фермент часто подвергается полной инактивации, и тогда торможение становится необратимым. Примером необратимого ингибирования является действие йодацетата, ДФФ, а также диэтил-и-нитрофенилфосфата и солей синильной кислоты. Это действие заключается в связывании и выключении функциональных групп или ионов металлов и молекуле фермента. [4]
Неконкурентное ингибирование легко выявить, построив для разных концентраций ингибиторов графики Лайнуивера - Бэрка ( рие. [5]
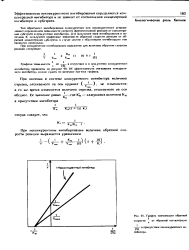 |
График зависимости обратной. [6] |
Эффективность неконкурентного ингибирования определяется концентрацией ингибитора и не зависит от соотношения концентраций ингибитора и субстрата. [7]
При неконкурентном ингибировании максимальная скорость реакции уменьшается, а константа Михаэлиса остается неизменной. [8]
При неконкурентном ингибировании аналогичные графики представляют собой семейство прямых ( рис. 2), пересекающихся с осью 1 / [ S ] в одной точке и отсекающих на ней отрезок, численно равный - 1 / & м - Это свидетельствует о том, что величина KM не изменяется при изменении концентрации неконкурентного ингибитора, тогда как величина тах при этом уменьшается. [9]
При неконкурентном ингибировании ингибитор не влияет на величину Км - На фиг. [10]
Этот тип неконкурентного ингибирования чаще всего наблюдается у ферментов, катализирующих превращения более одного субстрата, когда связывание ингибитора не блокирует связывание субстрата с активным центром. Ингибитор при этом соединяется как со свободным ферментом, так и с ES-комплексом. [11]
Проведенный нами анализ неконкурентного ингибирования нельзя считать полным, так как мы исходили из предположения, что константы равновесия / Ki для образования комплексов EI и ESI совпадают. Более того, возможен также другой механизм образования тройного комплекса: EI S EIS. Для подобной системы был проведен полный анализ при условии стационарности реакции. При этом был сделан следующий важный вывод: существование неконкурентных ингибиторов обычно означает, что константа Км является константой равновесия. [12]
 |
Действие конкурентного ингибитора ( схема по В.Л. Кретовичу. [13] |
Следует указать, что неконкурентное ингибирование также может быть обратимым и необратимым, поскольку отсутствует конкуренция между субстратом и ингибитором за активный центр. Примеры необратимого ингибирования приведены ранее. [14]
Известно [17], что неконкурентное ингибирование ферментативной активности а-химотрипсина борной кислотой обусловлено взаимодействием ингибитора с имидазольной группой остатка гистидина-57 активного центра фермента. Определить, принимает ли гистидин-57 активного центра фермента участие в связывании н-гексилборной кислоты. [15]
Страницы: 1 2 3 4