Конкурентный ингибитор
Cтраница 1
Конкурентный ингибитор - это молекула, настолько похожая по своей структуре на молекулу субстрата, что фермент не может различить их. В результате связывания конкурентного ингибитора с активным центром фермента падает концентрация истинных фермент-субстратных комплексов и скорость реакции. Ингибитор в продукт не превращается. Конкурентные ингибиторы увеличивают Кт реакции, но не влияют на Vmax. Роль ингибитора, поскольку он конкурирует с субстратом за активный центр, фактически сводится к разбавлению субстрата. Следовательно, для достижения скорости реакции, равной половине Утах, теперь требуется большая концентрация субстрата. Так как путем увеличения количества субстрата можно нейтрализовать действие ингибитора, Vmax не меняется. [1]
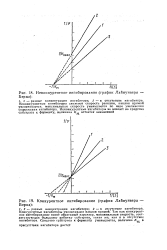 |
Неконкурентное - ингибирование ( график Лайнунвера - Берка.| Конкурентное ингибирование ( график Лайнуивера - Берка. [2] |
Конкурентные ингибиторы увеличивают наклон прямой. Так как конкурентное ингибирование имеет обратимый характер, максимальная скорость, соответствующая большому избытку субстрата, такая же, как и в Отсутствие ингибитора. [3]
 |
Необратимое ингибирование SH-фермента иодацетамидом. [4] |
Конкурентный ингибитор конкурирует с субстратом за связывание с активным центром, но в отличие от субстрата связанный с ферментом конкурентный ингибитор не подвергается ферментативному превращению. Отличительная особенность конкурентного ингибирования состоит в том, что его можно устранить или ослабить, просто повысив концентрацию субстрата. Например, если при заданных концентрациях субстрата и конкурентного ингибитора активность фермента подавлена на 50 %, то мы можем уменьшить степень ингибирования, повысив концентрацию субстрата. [5]
Конкурентные ингибиторы, по своей структуре напоминающие обычно субстрат, обратимо конкурируют с ним за связывание с активным центром, но в отличие от субстрата не претерпевают никаких превращений под действием фермента. Неконкурентные ингибиторы связываются не с активным центром, а с каким-то другим участком молекулы фермента. Они могут присоединяться как к свободному ферменту, так и к фермент-субстратному комплексу; их действие нельзя устранить путем добавления субстрата. Ферменты ускоряют химические реакции благодаря тому, что обеспечивают правильную ориентацию молекулы субстрата в непосредственной близости от каталитического центра, предоставляют для катализа протон-донорные и протон-акцепторные группы, образуют при помощи ковалентных связей нестабильные промежуточные соединения с субстратом и вызывают напряжение в молекуле субстрата или ее деформацию. Кроме каталитической активности не - которые ферменты обладают также и ре-гуляторной активностью. Они служат как бы дирижерами, задающими темп метаболическим процессам. Некоторые регуляторные ферменты, называемые ал-лостерическими, регулируют скорость реакций путем обратимого нековалент-ного присоединения специфических модуляторов, или эффекторов, к регулятор-ному, или аллостерическому, центру фермента. Такими модуляторами могут быть либо сами субстраты, либо какие-то промежуточные продукты метаболизма. К другому классу относятся регуляторные ферменты, способные изменять свою активность путем ковалентной модификации содержащихся в них специфических функциональных групп, необходимых для активности фермента. Некоторые ферменты существуют в нескольких формах, называемых изофермента-ми, которые различаются по своим кинетическим характеристикам. Многие генетические заболевания человека обусловлены нарушением в результате мутаций функционирования одного или нескольких ферментов. [6]
Конкурентные ингибиторы связываются в том же активном центре, что и субстраты, предотвращая взаимодействие фермента с субстратом уже на стадии связывания. При этом образуются комплексы, аналогичные комплексам Михаэлиса, но не способные к дальнейшим превращениям, или реагирующие очень медленно. В итоге фермент выводится из строя. [7]
Конкурентные ингибиторы отмечены звездочкой. [8]
 |
Схема образования активных и неактивных фермент-субстратных комплексов.| Влияние концентрации ацетилхолина на скорость его. [9] |
Конкурентные ингибиторы обратимого действия реагируют, как правило, со свободным активным центром, с к-рым реагирует субстрат, и не реагируют с фермент-субстратным комплексом. [10]
Конкурентный ингибитор лимитирующего фермента Еч будет вызывать накопление В точно так же, как и неконкурентный ингибитор, рассмотренный выше, но в этом случае регуляция системы может быть весьма эффективной и общая скорость процесса практически не изменится. Влияние конкурентных ингибиторов на другие ферменты системы будет, вероятно, столь же слабым. [11]
Канаванин как конкурентный ингибитор препятствует проникновению аргинина через клеточные мембраны и может встраиваться в белки вместо аргинина. [12]
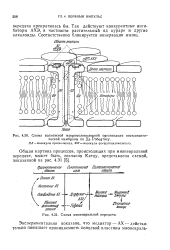 |
Схема возможной макромолекулярной организации постсинапти.| Схема миоиевральной передачи. [13] |
Так действуют конкурентные ингибиторы АХЭ, в частности растительный яд кураре и другие алкалоиды. Соответственно блокируется иннервация мышц. [14]
Кетоглутарат - конкурентный ингибитор реакции окисления М - метил - Ь - глутамата, катализируемой N-метилглута-мат - дегидрогеназой. [15]
Страницы: 1 2 3 4