Восстановление - анион
Cтраница 1
Восстановление аниона МпО - до катиона Mn2 сопровождается изменением окраски от фиолетовой до светло-розовой или бесцветной. [1]
Восстановление анионов XOJT, ХОГ, ХОГ ( Х С1 Вг, I), как правило, происходит ступенчато. Первые необратимые ступени протекают с участием нескольких электронов и образованием свободных галогенов. Вторая ступень одноэлектронна, продуктом ее является галогенид-ион. На скорость протекающих электродных процессов большое влияние оказывает природа фонового электролита. В замедленной стадии переноса электрона принимают участие нейтральные молекулы растворителя. [2]
Восстановление анионов азотной кислоты протекает легче, чем выделение водорода. [3]
 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [4] |
Подробнее восстановление анионов рассмотрено в Дополнениях ( см. стр. [5]
Кинетика восстановления анионов второй группы существенным образом зависит от природы донора протонов, в качестве которых могут выступать адсорбированные на поверхности электрода молекулы растворителя, катионы NH4 и НзО и другие частицы. [6]
 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [7] |
Реакции восстановления анионов тормозятся органическими молекулами и анионами и не тормозятся органическими катионами. [8]
Процесс восстановления анионов отличается специфическими особенностями, так как поверхность электрода заряжена отрицательно. Многие анионы, например NCXj, NO -, BrO -, JCXJ -, восстанавливаются в присутствии однозарядных катионов при очень отрицательных потенциалах. При прибавлении в раствор поливалентных катионов ( Са2, La3, Th4) потенциал их восстановления сдвигается к более положительным значениям и реакция идет с большей скоростью. Это особенно отчетливо наблюдается при восстановлении S2Og - на ртутном капельном электроде ( см. стр. При этом, если процесс не начинается до достижения потенциала нулевого заряда, то он либо совсем не протекает, либо протекает при очень отрицательных потенциалах. Если же процесс восстановления начинается до достижения потенциала нулевого заряда, то, после того как этот потенциал достигнут, вместо сил притяжения между поверхностью электрода и анионами начнут действовать силы отталкивания и процесс может замедлиться или совсем прекратиться. [9]
Механизм восстановления аниона в устойчивый продукт детально не установлен, но общее изменение валентности должно быть результатом ряда последовательных стадий. Следует отметить, что азотная кислота не является специфическим реагентом, и поэтому большое значение имеет выбор соответствующих экспериментальных условий. [10]
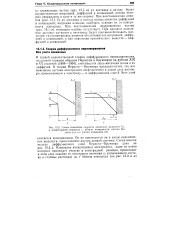 |
Схема изменения скорости движения жидкости t / ь. [11] |
При восстановлении анионов ( рис. 15.1 6) их доставка к катоду осуществляется диффузией и конвекцией; миграция анионов, наоборот, отводит их от поверхности электрода. При восстановлении незаряженных частиц ( рис. 15.1 е) миграция вообще отсутствует. При анодном окислении доставке катионов к электроду будет противодействовать миграция; транспортировка анионов обеспечивается миграцией, диффузией и конвекцией, а при окислении органических веществ - диффузией и конвекцией. [12]
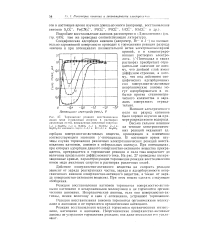
При восстановлении анионов наблюдаются часто аномальные явления и иного порядка. Из этого рисунка видно, что восстановление аниона S2082 начинается при относительно положительных значениях потенциала. На кривой имеется ярко выраженный перегиб, соответствующий предельному диффузионному току. Однако увеличение потенциала катода приводит к необычным явлениям. Ток восстановления начинает резко падать, достигая малой величины. Последнее показывает, что восстановление персульфат-иона замедляется. [13]
При восстановлении анионов PtCllT в присутствии катионов ТБА /, / - кривые имеют более сложную форму, чем при восстановлении анионов персульфата и феррицианида, а именно после резкого возрастания ток падает и становится меньше предельного диффузионного тока. Первоначальный подъем тока вызван сдвигом % - потенциала в положительную сторону, а последующий спад тока связан с блокировкой поверхности органическими катионами. Сдвиг о) 1-потенциала в отрицательную сторону при адсорбции органических анионов ускоряет электровосстановление катионов. [14]
Сначала производят восстановление аниона щавелевой кислоты в анион гликолевой кислоты. [15]
Страницы: 1 2 3 4