Восстановление - катион
Cтраница 2
При восстановлении катионов, а также в случае электродных процессов, скорость которых определяется предшествующей при-электродной протонизацией незаряженных частиц, увеличение порядкового номера катиона щелочного металла индифферентного электролита приводит к замедлению процесса. Жданов и Зуман [210] наблюдали снижение высоты каталитической волны в растворах N-тропониламинокислот при увеличении размера катиона фона. [16]
Сравнительная легкость восстановления катиона до свободного металла зависит, главным образом, от положения последнего в ряду напряжений. Чем левее в этом ряду стоит металл, тем он, как правило, химически более активен и тем легче переходит в состояние иона; наоборот, чем он расположен правее, тем он менее химически активен и тем. Определяя положение элементов группы сероводорода в ряду напряжений, видим, что все они, за исключением Cd, Sn, Pb, расположены правее водорода. Поэтому отвечающие им катионы сравнительно легко восстанавливаются до металла. [17]
Сравнительная легкость восстановления катиона до свободного металла зависит, главным образом, от положения последнего в ряду напряжений. Определяя положение элементов группы сероводорода в ряду напряжений, видим, что все они, за исключением Cd, Sn, Pb, расположены правее водорода. Поэтому отвечающие им катионы сравнительно легко восстанавливаются до металла. Реакции этого типа имеют в аналитической практике большое значение, так как очень часто представляют собой наиболее простой прием открытия соответствующего катиона. [18]
Сравнительная легкость восстановления катиона до свободного металла зависит, главным образом, от положения последнего в ряду напряжений. Определяя положение элементов группы сероводорода в ряду напряжений, видим, что все они, за исключением Cd, Sn, Pb, расположены правее водорода. Поэтому отвечающие им катионы сравнительно легко восстанавливаются до металла. Реакции этого типа имеют в аналитической практике большое значение, так как очень. [19]
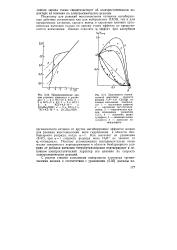
Суммарный ток восстановления катионов М и кислорода / i t o, на рис. 86 представлен пунктирной кривой. [20]
Суммарный ток восстановления катионов М и кислорода г 10г на рис. 86 представлен пунктирной кривой. [21]
Суммарный ток восстановления катионов М и кислорода / i t o, на рис. 86 представлен пунктирной кривой. [22]
В случае восстановления катиона на жидком ртутном катоде с образованием амальгамы потенциал электрода будет сдвигаться - не только за счет изменения концентрации разряжающихся ионов в растворе, но и за счет изменения концентрации металла в электроде. [23]
На катоде происходит восстановление катионов. Естественно, что первыми будут восстанавливаться те катионы, которые сильнее притягивают к себе электроны и прочнее их удерживают. Способность катионов металлов к восстановлению определяется положением металла в электрохимическом ряду напряжений. [24]
Ими было исследовано восстановление катионов, анионов и нейтральных молекул на капельном ртутном электроде в присутствии адсорбирующихся органических катионов, анионов и нейтральных молекул, а также неорганических поверхностно-активных анионов. [25]
На катоде происходит восстановление катионов меди, поскольку она восстанавливается. Из уравнения реакций следует, что если на аноде выделяется 22 4 л кислорода, то на катоде восстанавливается 128 г меди, если на аноде 2 8 л, то на катоде х г меди. [26]
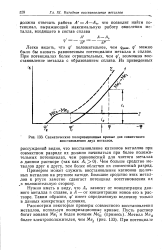 |
Схематические поляризационные кривые для совместного восстановления двух металлов. [27] |
Примером может служить восстановление катионов щелочных металлов на ртутном катоде. Большое сродство этих металлов к ртути заметно сдвигает потенциал восстановления их в положительную сторону. [28]
Восстановители Сравнительная легкость восстановления катиона до свободного металла зависит, главным образом, от положения последнего в ряду напряжений. Определяя положение элементов группы сероводорода в ряду напряжений, видим, что все они, за исключением Cd, Sn, Pb, расположены правее водорода. Поэтому отвечающие им катионы сравнительно легко восстанавливаются до металла. [29]
Страницы: 1 2 3 4