Восстановление - растворенный кислород
Cтраница 2
Оборудование газофракционирующих установок - абсорберы, трубчатые печи, теплообменники, подогреватели-кипятильники и др. - подвергаются коррозионному расслоению металла вследствие наводораживаю-щего действия дренажных вод, содержащих сероводород. При очистке масляного сырья избирательными растворителями характерна коррозия металлов в воднокрезольных смесях с восстановлением растворенного кислорода. [16]
Даже аналогия с гальваническими элементами опасна, поскольку катодные реакции в контактирующих парах представляют собой либо восстановление кислорода, либо выделение водорода, но не осаждение металла. Медь обычно не выделяет водород, и в контактной паре катодной реакцией является обычно восстановление растворенного кислорода. Во многих случаях, когда среда изолирована от воздуха например в установках центрального отопления, первоначально содержавшийся в растворе кислород быстро расходуется и не возобновляется, так что контактный ток снижается до пренебрежимо малой величины. В таких условиях медь и сталь можно употреблять в контакте друг с другом. [17]
Для гальванической ванны, к которой относятся данные приведенные на рис. 6.4, потенциал меди составляет 0 042 В. Длительное нахождение деталей в гальванической ванне приводит лишь к слабому растворению меди, сопровождающемуся восстановлением растворенного кислорода в качестве катодной реакции. Это растворение не мешает получению удовлетворительного никеля покрытия и полностью подавляется в случае погружения деталей в ванну под током. Проблема нанесения подслоя меди решается путем использования комплексной медноцианистой ванны. [19]
Реакции (4.97) и (4.98) характеризуют кислородную коррозию, а (4.99) - щелочную коррозию, поскольку наиболее часто сопряженным процессом эта реакция является в щелочных растворах. На рис. 4.40 представлены поляризационные кривые, когда катодным сопряженным процессом являются реакции выделения водорода из воды и восстановления растворенного кислорода. При этом выделение водорода из воды происходит по механизму замедленного разряда, а восстановление кислорода имеет сложный механизм: со сдвигом потенциала в катодную сторону последовательно реализуются механизм замедленного разряда, а затем смешанный и диффузионный механизмы. [20]
Этот метод имеет преимущества перед полярографическим: результаты его не зависят от характеристики капилляра, среды присутствия посторонних ионов [2, 16], изменения температуры в пределах нескольких градусов, а главное - амперометрически могут определяться вещества, которые сами не восстанавливаются, а восстанавливается титрующий реагент и ряд других элементов. Особенно перспективны вольфрамовый ( методика № 60) и графитовый [32], поскольку поверхность их легко очищается, а посторонние процессы, напри-мер восстановление растворенного кислорода, проходят при более отрицательных потенциалах, чем на платине. [21]
 |
Электрические схемь. [22] |
Каждый раз при изменении потенциала наблюдается бросок тока, который затем, через определенные промежутки времени, достигает некоторого постоянного значения. По его величине строится полярограмма. Потенциал восстановления растворенного кислорода на твердом электроде лежит между 0 5 и 0 9 в. Факторы, от которых зависит размер плато, были рассмотрены выше. [23]
По литературным данным, из всех циклических перекисей кетонов полярографическим методом исследована только триперекись ацетона. Авторы отмечают, что волна восстановления растворенного кислорода накладывается на волну триперекиси и мешает полярографическому опреде - 1 мка лению последней. [24]
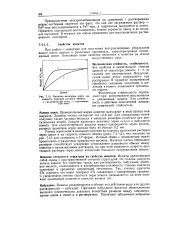 |
Влияние величины зерен на скорость реакции ионного обмена. [25] |
Преимуществом электронообменников по сравнению с растворимыми редокс-системами является тот факт, что они не загрязняют раствор - Ре3 - ион восстанавливается в Ре2 - ион, а гидрохинон окисляется в хинон. Применяя подходящий восстановитель, можно перевести смолу в ее исходное состояние. В технике эти смолы применяют для восстановления растворенного кислорода. [26]
Кривые имеют форму а. При титровании будет наблюдаться заметный остаточный ток, так как при указанных потенциалах возможно восстановление растворенного кислорода, который авторы метода не удаляют. [27]
Для протекания этой реакции на катодном участке должен одновременно происходить процесс восстановления, заключающийся & приобретении электронов. При катодной реакции поглощаются электроны, поставляемые в процессе окисления. Анодная реакция не сможет протекать, если эти электроны не будут поглощаться. Восстановление растворенного кислорода и выделение газообразного водорода в результате восстановления ионов водорода ( в частности, из кислых растворов) относятся к двум самым обычным реакциям, протекающим при коррозии металлов в водных средах. [28]
МИЭ), присоединяя платиновый электрод к положительному: полюсу источника тока. При этом потенциале медь на электроде не выделяется и титрование протекает не только совершенно нормально, но даже лучше, чем в чистых растворах хлорида калия ( или натрия) при потенциале меркур-иодидного или насыщенного каломельного электрода. КЭ) практически не происходит восстановление растворенного кислорода, который легко восстанавливается на платиновом электроде при более отрицательных потенциалах, особенно в кислых растворах. Кольтгоф и Курода2, работая с насыщенным каломельным электродом без наложения внешнего напряжения, продувают раствор азотом при титровании малых количеств хлорид-иона в кислых растворах. При 0 4 в ( МИЭ) эта операция не нужна. [29]
МИЭ), присоединяя платиновый электрод к положительному полюсу источника тока. При этом потенциале медь на электроде не выделяется и титрование протекает не только совершенно нормально, но даже лучше, чем в чистых растворах хлорида калия ( или натрия) при потенциале меркур-иодидного или насыщенного каломельного электрода. КЭ) практически не происходит восстановление растворенного кислорода, который легко восстанавливается на платиновом электроде при более отрицательных потенциалах, особенно в кислых растворах. Кольтгоф и Курода2, работая с насыщенным каломельным электродом без наложения внешнего напряжения, продувают раствор азотом при титровании малых количеств хлорид-иона в кислых растворах. При 0 4 в ( МИЭ) эта операция не нужна. [30]
Страницы: 1 2 3
