Восстановление - окись - железо
Cтраница 3
Закись железа FeO получают восстановлением пз окиси железа ( через закись-окись) или окислением металлического железа. Процесс восстановления проводят обычно при 700 - 800 С. [31]
Как устроена вращающаяся печь для восстановления окиси железа. [32]
Полученные данные и уравнения кинетики восстановления окиси железа в присутствии железных порошков используются для расчетов технических параметров в производственной практике. [33]
Хорошие результаты дает старый способ восстановления окиси железа водородом. [34]
Активные железные массы, полученные восстановлением окиси железа в присутствии железных порошков или окалины, содержащей избыточную закись железа, и испытанные на срок службы в течение 950 циклов в аккумуляторах ТЖН-350, показали высокую отдачу по емкости ( до 150 % ( номинальной) при потенциале железного электрода в пределах 0 44 - 0 46 в по Zn вспомогательному электроду. [35]
Применяя высокоактивные препараты, полученные восстановлением окиси железа при 450 С, авторы обнаружили, что реакция протекает с заметной скоростью лишь при температурах выше 350 С. [36]
Руденко и С. Т. Ростовцеву [243] при восстановлении окиси железа добавка Нз и СО также ускоряет ( при 600 С) распад окиси углерода. Однако, в этих условиях наибольшее количество элементарного углерода появляется при работе со смесью, содержащей 10 % Нз и 90 % СО. [37]
При этой температуре обе реакции: восстановление окиси железа водородом и окисление железа водой ( коррозия) - равновероятны. [38]
Совершенно чистое железо может быть получено восстановлением окиси железа водородом или электролизом некоторых его солей. [39]
Чистое металлическое железо может быть получе-но путем восстановления окиси железа Ре20з водородом при нагревании. В настоящее время разработаны методы, которые позволяют получить железо, содержащее 10 - 6 % примесей. [40]
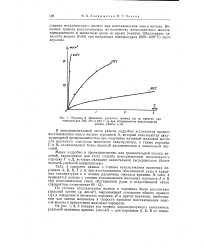 |
Порошок А. Изменение удельного привеса ( q во времени при. [41] |
В экспериментальной части работы подробно исследуется процесс восстановления окиси железа порошком А, который используется аккумуляторной промышленностью при получении активной железной массы для железного электрода щелочного аккумулятора, а также порошки Б и В, отличающиеся более высокой дисперсностью и химической чистотой. [42]
 |
Изменение степени восстановления окиси железа с течением времени при вое-становлении окисью углерода ( 1 и водородом ( 2. [43] |
Приведенное выше экспериментальное доказательство условий протекания реакций восстановления окиси железа подтверждается теоретически. [44]
Изучение влияния концентрации углерода на скорость процесса восстановления окиси железа ( Гв20з) при 1100 С показало, что с увеличением содержания углерода в навеске от 15 % до 25 - 35 % наблюдается снижение скорости восстановления в начальные промежутки времени. [45]
Страницы: 1 2 3 4