Восстановление - ртуть
Cтраница 2
Реакция в водном растворе немедленно приводит к восстановлению ртути до металла. Устойчивость этих соединений возрастает в следующем порядке: Cl Br J CN. Моногидразинаты галогенидов двухвалентной ртути вступают в реакцию с водой, причем чем менее устойчивы эти соединения, тем легче они реагируют. В результате реакции образуются сольво-основные соединения. Вещество ClHgN2H2HgCl легко получается при медленном добавлении ацетата натрия к раствору, содержащему хлорид двухвалентной ртути и сульфат гидразина. Оно представляет собой неустойчивое вещество желтого цвета, взрывающееся при нагревании или при ударе. В результате взаимодействия с уксусным ангидридом получается вещество с суммарным составом, соответствующим формуле HgN2Ac2, которое при обработке сероводородом дает диацетилгидразин. [16]
В присутствии олова ( П) вначале происходит восстановление ртути ( Н) до ртути ( 1) и выделяется белый осадок каломели Н § 2С12, постепенно чернеющий вследствие образования тонкодисперсной металлической ртути при дальнейшем восстановлении ртути ( 1) оловом ( П) до металлической ртути. [17]
Мазь при хранении на свету чернеет вследствие реакции восстановления ртути амидохлорида резорцином до металлической ртути. Лекарство отпуску не подлежит. [18]
Большинство соединений Pt4, Pt2 восстанавливается непосредственно от потенциала восстановления ртути. [19]
Электрохимическое поведение, кинетика окисления ртути ( I) и восстановления ртути ( II) хорошо изучены. Установлены оптимальные значения Ер. [20]
 |
Примерная структура потерь ртути в производстве хлора методом с ртутным катодом. [21] |
Для регенерации ртути в жидких отходах могут быть использованы методы восстановления ртути до металлической и отделения ее центрофугированием или фильтрованием. Однако и в этом случае остаточное содержание ртути будет не ниже 0 03 - 0 05 г / л жидких стоков, поэтому такие методы непригодны для санитарной очистки. [22]
При этом используют способность ДМК окисляться в присутствии хлорида ртути с восстановлением ртути до элементного состояния. Конец трубки изогнут вниз и заканчивается ситчатым дном. Трубка подогревается двумя микропечами типа СУОЛ-015 длиной 6 и 20 см. В широкую часть трубки помещают кварцевую лодочку размером 0 7X13 см с образцом. Узкая часть трубки служит для дополнительного сжигания твер дых частиц, выделившихся при нагревании образца. К навеске пробы 50 - 500 мг добавляют 500 мг оксида магния и 50 мг оксида ванадия ( V) и смесь тщательно растирают в агатовой ступке. Оксид магния предварительно прокаливают 1 ч при 1100 С для удаления следов ртути. Температура второй печи 800 С, температура первой печи сначала 100 С, затем в течение 5 - 6 мин ее повышают до 800 С. [23]
Ион Р20 - дает волну восстановления, идущую сразу за анодной волной восстановления ртути. Площадка предельного тока хорошо выражена до - 0 3 в. В интервале от - 0 6до - 1 2 наполярограм-ме наблюдается максимум. [24]
При определении ртути в присутствии висмута в одном и том же растворе по окончании восстановления ртути начинает восстанавливаться трехвалентный висмут. [25]
Муравьиная кислота обладает восстановительными свойствами, поэтому - при нагревании ртутной соли муравьиной кислоты происходит восстановление ртути до свободного металла. [26]
В основу метода определения следов примесей в ртути, предложенного Мейером [965], положено отделение ртути от электроотрицательных металлов восстановлением ртути из азотнокислого раствора муравьиной кислотой. Содержание Zn, Cd, Pb и Си определяют полярогра-фически; Mn, T1 и Mg определяют методом пламенной фотометрии; Fe, Co, Ni и Bi - фотометрически. Метод позволяет одновременно анализировать четыре образца за 8 5 час. [27]
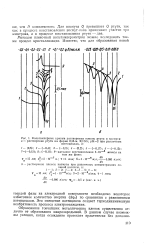 |
Вольтамперные кривые растворения пленок ртути и висмута. а - растворение ртути на форме 0 25 - м. KCNS. рН2 при различных потенциалах, в. [28] |
Для висмута Q превышает Q ртути, так как в процессе восстановления висмут-иона принимают участие три электрона, а в процессе восстановления ртути - два. [29]
Чувствительность определения 2 - 10-в % при навеске 1 г. Метод основан на предварительной химической подготовке, включающей растворение пробы в серной кислоте в присутствии перманганата, восстановление ртути до металлической SnCl2 и перевод ее в кювету фотометра ( длина 30 см) током воздуха. [30]
Страницы: 1 2 3 4