Восстановление - ртуть
Cтраница 3
 |
Блок-схема РАФ-Ш. [31] |
Процесс измерения содержания ртути в твердых пробах состоит из двух операций: 1) термическая возгонка ртути из пробы в печи при 700 С и поглощения паров ртути сорбентом, 2) восстановление химически связанной ртути в сорбенте до металлической, перевод ее в газовую фазу потоком воздуха с последующим прокачиванием воздуха с парами ртути через измерительную кювету. [32]
Ртуть ( II) восстанавливают до Hg хлоридом олова и металлической медью. Восстановление ртути ( II) SnCl2 в зависимости от среды протекает с образованием различных продуктов реакции. [33]
Адсорбированная на поверхности ртутного электрода пленка бромида свинца характеризуется [1248] селективной проницаемостью к различным деполяризаторам, в том числе и к ртути. Она тормозит восстановление ртути и не влияет на процесс восстановления серебра. Это использовано для определения серебра в присутствии - 5-кратного избытка ртути на фоне 1М раствора NaBr 10 - 3 М раствора свинца по i - f - кривой, снятой при - 0 27 в. Измерение диффузионного тока проводят в конце жизни капли. В присутствии 5 - 10 - 3Af раствора свинца определению серебра не мешает 75-кратный избыток ионов ртути. [34]
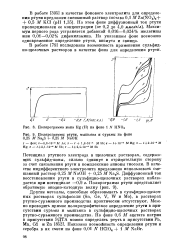 |
Полярограмма иона Hg ( II на фоне 1 N HNO3.| Полярограммы ртути, мышьяка и сурьмы на фоне 0 25 М Na2S 0 25 М NaOH. [35] |
Потенциал ртутного электрода в щелочных растворах, содержащих сульфид-ионы, сильно сдвинут в отрицательную сторону за счет связывания ртути в комплексные анионы тиосоли. Диффузионный ток восстановления ртути в сульфидно-щелочных растворах наблюдается при потенциале - 0 9 в. [36]
Для определения ртути могут быть использованы различные фоны. Изучено окисление и восстановление ртути ( I) на фоне 1 М НСЮ4 [203, 204] с использованием стационарного ртутного электрода. [37]
Восстановление ртути из киновари происходит за счет окисления серы кислородом воздуха при 600 - 850 С. Иногда применяют способ восстановления ртути из ее сернистых соединений нагреванием в ретортах с железом или известью. [38]
ДТПА) и анализируемый металл вытесняет ион ртути из комплекса. Измеряемый ток возникает при восстановлении ртути. [39]
Осадок становится заметным только тогда, когда содержание ртути в 25 мл раствора достигает примерно 2 мг. Если же титровать по току восстановления ртути ( II), при потенциалах 0 5 в и менее положительных 2 3, то возможны осложнения хода кривых вследствие некоторых побочных электродных реакций, а именно: если потенциал платинового электрода установить равным 0 5 в и несколько ниже, до 0 3 в ( МИЭ), то электрод покроется металлической ртутью. Если установить еще более отрицательный потенциал - например, 0 2 в или 0 1 в ( МИЭ) - то на кривых титрования вообще не будет перелома в конечной точке, так как при таких потенциалах происходит второй катодный процесс - непосредственное восстановление ртути II из взвешенных в растворе частиц иодида ртути ( II), образующихся во время титрования. В результате катодный ток понижается под конец титрования очень незначительно, так как вместо ионов ртути ( II), концентрация которых убывает, появляются частицы иоди да ртути, количество которых увеличивается. [40]
Осадок становится заметным только тогда, когда содержание ртути в 25 мл раствора достигает примерно 2 мг. Если же титровать по току восстановления ртути ( II), при потенциалах 0 5 в и менее поло -, жительных 2 3, то возможны осложнения хода кривых вследствие некоторых побочных электродных реакций, а именно: если потенциал платинового электрода установить равным 0 5 0 и несколько ниже, до 0 3 в ( МИЭ), то электрод покроется металлической ртутью. Если установить еще более отрицательный потенциал-например, 0 2 в или 0 1 в ( МИЭ) - то на кривых титрования вообще не будет перелома в конечной точке, так как при таких потенциалах происходит второй катодный процесс - непосредственное восстановление ртути II из взвешенных в растворе - частиц иодида ртути ( II), образующихся во время титрования. В результате катодный ток понижается под конец титрования очень незначительно, так как вместо ионов ртути ( II), концентрация. [41]
В качестве восстановителя Розе применял не чистую фосфористую кислоту, а продукт окисления желтого фосфора на влажном воздухе, содержащий некоторое количество фосфорной кислоты, которая, однако, не мешает. Азотная кислота, по мнению Розе, не мешает восстановлению ртути до каломели. [42]
Для выделения ртути из образца обычно пробу сжигают, а продукты сгорания пропускают через поглотитель, где задерживается только ртуть. Широко применяют также кислотную обработку пробы в сочетании с нагревом, восстановление ртути ( например, хлоридом олова или тетрагидроборатом натрия) и концентрирование ртути в поглотителе. Процесс выделения ртути из пробы обычно длится долго, а из поглотителя при нагреве вся ртуть удаляется в течение нескольких минут. Благодаря этому получают интенсивный аналитический сигнал. Кроме того, при накоплении ъ поглотителе в виде амальгамы ртуть освобождается от основной части продуктов сгорания или раствора. Вследствие этого устраняются помехи, что также способствует повышению чувствительности и точности анализа. Однако небольшое количество сопутствующих веществ все же задерживается поглотителем. Для освобождения от них практикуются двукратное амальгамирование и возгонка ртути. Сначала ртуть задерживают первым поглотителем, затем присоединяют к нему второй поглотитель, первый поглотитель нагревают и газом-носителем транспортируют ртуть во второй поглотитель. [43]
Ионы Pd2, не образующие комплексов, и некоторые комплексы ( ацет. Cl, CNS, гексаметилентетрамин и др.) восстанавливаются непосредственно до потенциала восстановления ртути. [44]
Описан метод определения Hg, основанный на измерении конц-ции ее паров в газах по атомной абсорбции резонансного излучения Hg при длине волны 2537 А. Определение Hg в солях NaCl, NaNOg, КС1, KNO3, KMnO4 проводили восстановлением ионной ртути в р-ре исследуемой соли до металлич. Метод применим для водор-римых солей. [45]
Страницы: 1 2 3 4