Восстановление - сера
Cтраница 2
Здесь примечательно восстановление серы до четырехвалентной за счет окисления атома углерода, получившего в результате реакции связь с кислородом. [16]
 |
Процессы очистки от активной серы и обработки. [17] |
С помощью восстановления серы удаляется сероводород из потоков сернистых газов и углеводородов. [18]
Ферментативные пути восстановления серы в ФАФС детально изучены только у нескольких организмов. [19]
Первоначально на установках восстановления серы из сероводорода широкое применение нашли природные бокситы, состоящие в основном из оксидов алюминия и железа. Использование боксита как катализатора на ранней стадии развития процесса было обусловлено, в первую очередь, его дешевизной. [20]
Речь идет о восстановлении серы из серной кислоты. [21]
Определение основано на восстановлении серы раствором Ti ( III) и поглощении сероводорода 4 - 5N раствором КОН. [22]
От чего зависит степень восстановления серы. [23]
Промежуточные и побочные продукты восстановления серы ( сероокись углерода, сероуглерод, сероводород) подвергаются каталитическому превращению с образованием элементарной серы в контактных аппаратах с катализатором на основе окиси алюминия. Высокотемпературный катализатор работает в интервале температур 420 - 440 С, а низкотемпературный - в интервале 200 - 220 С. [24]
Печные газы обрабатываются углеродом для восстановления серы из газов. В шихту, в количестве 10 - 12 % дается кокс в кусках размером 10 - 15 мм. Наличие такого кокса приводит к увеличению поверхности и усилению взаимодействия серосодержащих газов с углеродом. Высшие сульфиды: пирит FeS2, халькопирит CuFeS2, ковеллин CuS, борнит Cu5FeS4 диссоциируют с образованием низших сульфидов и парообразной серы. В дальнейшем сульфиды окисляются с образованием окислов и сернистого газа. [25]
Тем не менее механизм процессов восстановления серы до конца не выяснен. [26]
Иодометрическое определение серы обычно проводится восстановлением серы до сульфида и иодометрическим титрованием последнего. Выделяющийся сероводород поглощают аммиачным раствором хлорида кадмия; сульфид кадмия подкисляют и проводят иодометрическое титрование. [27]
СО удаляется в атмосферу и возможность восстановления серы исключается. Окончательное раскисление ведут за 2 - 3 мин до выпуска металла путем введения в металл 0 4 - 1 0 кг / т алюминия или до 1 кг / т силикокальция. [28]
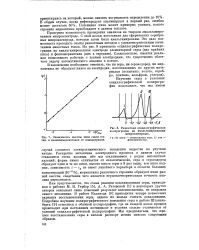 |
Зависимость высоты пика смеси геп-тил - и изоамилмеркаптанов от концентрации. [29] |
Нам представляется, что схема реакции восстановления серы, приводимая в работах М. И. Гербер 15 ], А. А. Ратовской [1] и некоторых других авторов описывает лишь конечный результат восстановления, не вскрывая самого механизма. В работе Кальвода [6] приводится четыре возможных варианта восстановления серы, однако их нельзя считать доказанными. Подробное изучение полярографического поведения серы в работе Штакель-берга [9] относится к обычной полярографии, где на каждой капле процесс происходит при постоянном потенциале и условия сильно отличаются от условий осциллографической полярографии. Мы предполагаем, что процесс восстановления серы в кислом растворе можно описать следующим образом. [30]
Страницы: 1 2 3 4