Восстановление - сера
Cтраница 3
СО удаляется в атмосферу и всякая возможность восстановления серы исключается. [31]
Окисление железа происходит за счет серы, а восстановление серы за счет железа. Окислителем в этой реакции является сера - она принимает электроны, а восстановителем - железо - оно отдает электроны. [32]
В процессе сплавления может происходить как окисление, так и восстановление серы. [33]
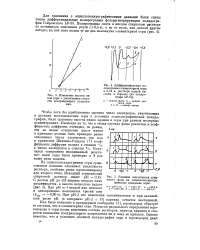
Чтобы хотя бы приближенно оценить число электронов, участвующих в реакции восстановления серы в условиях осциллографической полярографии, были сравнены высоты пиков кадмия и серы при равных молярных концентрациях. Получился совершенно неожиданный результат: пики серы были примерно в 8 раз выше пика кадмия. [35]
Для определения условий анализа серы в элементарном селене произведены термодинамические расчеты реакций восстановления серы до сероводорода. [36]
 |
Процессы очистки от активной серы и обработки. [37] |
Как окисление, так и восстановление используется для обработки остаточного газа, поступающего из установок восстановления серы, в зависимости от состава газа и экономических условий нефтеперерабатывающего завода. Окислительные процессы сжигают остаточный газ с целью преобразования всех сернистых соединений в двуокись серы, а процессы перегонки преобразуют сернистые соединения в сероводород. [38]
Нераг test ( качественная) проба на серу; - сплавляют смесь испытуемого образца, едкого натра и угля с целью восстановления серы в Na2S, полученную массу помещают на серебряную пластинку и смачивают водой; потемнение пластинки указывает на присутствие серы. [39]
Как показано Квартирмейном и Хиллом [21], при взаимодействии Ti ( III) в растворе концентрированной ортофосфорной кислоты с соединением серы любой валентности реакция протекает до восстановления серы до сульфид-иона. Образующийся сероводород поглощается раствором щелочи, в которой сульфид-ион отличается наибольшей химической устойчивостью. [40]
Уголь используется не только как восстановитель, но служит также для достижения более высокой температуры в печи ( до 1350 С), что необходимо для лучшего восстановления серы. [41]
Мне казалось, что для исследования активирования водорода в высшей степени чувствительная и легко поддающаяся количественному определению реакция восстановления нитрата в нитрит гораздо более пригодна, чем восстановление серы в сероводород. А что трехатомный водород, который восстанавливает серу в сероводород, способен также восстанавливать нитрат в нитрит - в этом как будто не было основания сомневаться. [42]
Образование сероводорода из серы, содержащейся в тканях, наблюдалось французскими исследователями еще во второй половине XIX века; однако только в 1907 г. Гефтер [285] установил, что восстановление серы белками и сульфгидрильными производными является стехиометрической, а не каталитической реакцией. [43]
Сульфидные катализаторы, содержащие металлы VIII группы периодической системы элементов и осерненные H2S или в процессе гидрокрекинга сернистого сырья, рекомендуется [77] регенерировать в три ступени: 1) восстановление серы при 400 - 590 С любым водородсодержащим газом до постоянного ее уровня в течение 1 ч ( не менее); 2) окисление кислородсодержащим топочным газом при 315 - 649 С для снятия коксовых отложений; 3) вторичное восстановление в менее жестких условиях. [44]
В действительности, как показал анализ продуктов перегонки, в парообразной фазе NH3: ( S03 - f - S02) l: 1.19. Это свидетельствует о том, что восстановление серы до четырехвалентного состояния происходит не только по приведенному выше уравнению. [45]
Страницы: 1 2 3 4