Восстановление - хлорат
Cтраница 3
Технический диоксид хлора производят на промышленных предприятиях ( химические и целлюлозно-бумажные комбинаты) в виде водного раствора восстановлением хлората натрия NaClO3 в кислой среде ( НС1, H2SO4) хлоридами или диоксидом серы. Этот метод получения технического СЮ2 экономически оправдан только при потребности в диоксиде хлора на уровне 50 кг / ч и отличается сложностью аппаратурного оформления технологической схемы и блокировок, требует высокой квалификации персонала, что делает нерациональным его практическое внедрение непосредственно на объектах ВКХ. [31]
Поэтому при использовании катодов из обычной углеродистой стали рекомендуется вводить в электролит небольшие добавки би-хромата натрия, предотвращающие восстановление хлората в результате уменьшения адсорбции на электроде ионов СЮз - Если в качестве катода применяют платину, никель или нержавеющую сталь, то восстановление хлората не происходит. [32]
Хлористый кальций и хлористый магний совместно или раздельно добавляют к электролиту для повышения выхода по току путем уменьшения степени восстановления хлоратов и гипохлори-тов на катоде. [33]
В тех случаях, когда используют платиновые или платино-титановые аноды, в раствор вводят буферирующую добавку бихромата ( до 5 г / л), которая одновременно предупреждает восстановление хлората на катоде. [34]
Прямое восстановление хлоратов в хлориты не может дать эффекта, так как при этом образуются хлориды, однако, можно получить хлориты из двуокиси хлора, приготовленной путем восстановления хлоратов, при последующей обработке СЮ2 щелочью или перекисью натрия. [35]
В тех случаях, когда используют платиновые или платино-титановые аноды, в раствор вводят буферирующую добавку бихромата ( до 5 г / л), которая одновременно предупреждает восстановление хлората на катоде. [36]
В том случае, когда установку используют для плавки каустической соды, полученной диафрагменным методом, в бак 14 из напорного бачка 18 добавляют раствор сахарозы, что способствует восстановлению хлоратов. [37]
Следовательно, для рассматриваемого ряда термодинамически благоприятными являются все реакции восстановления хлората сернистым ангидридом, в том числе прямое восстановление до двуокиси хлора, но наиболее устойчивая система образуется при восстановлении хлората до хлорида. [38]
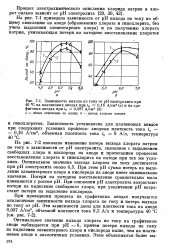
На рис. 7 - 2 показано изменение потерь выхода хлората натрия по току в зависимости от рН электролита, связанное с выделением свободных хлора и кислорода на аноде и протеканием процессов восстановления хлората и гипохлорита на катоде при тех же условиях. При этом рН сумма потерь на выделение элементарного хлора и кислорода на аноде имеет минимальное значение. При снижении рН электролита возрастают потери на выделение свободного хлора, при увеличении рН возрастают потери на выделение кислорода. [40]
Поэтому при использовании катодов из обычной углеродистой стали рекомендуется вводить в электролит небольшие добавки би-хромата натрия, предотвращающие восстановление хлората в результате уменьшения адсорбции на электроде ионов СЮз - Если в качестве катода применяют платину, никель или нержавеющую сталь, то восстановление хлората не происходит. [41]
Восстановление хлората может быть проведено сернистым газом, азотистой кислотой или цинковой пылью в уксуснокислом растворе при кипячении. [42]
Методы определения хлоратов в большинстве случаев осиоваен на восстановлении их с последующим оксждиметрическнм определение избытка восстановителя. Восстановление хлоратов протекает очень меддевно и требует применения катализаторов. [43]
Восстановление хлората может быть проведено сернистым газом, азотистой кислотой или цинковой пылью в уксуснокислом растворе при кипячении. [44]
Превалирующей является первая реакция, идущая со значительно большей ( в 100 - 1000 раз) скоростью, чем другие. При восстановлении хлоратов хлоридами теоретически не расходуется активный хлор, так как наряду с двуокисью хлора образуется молекулярный хлор, который также обладает активными окислительными ( отбеливающими) свойствами. [45]
Страницы: 1 2 3 4