Восстановление - цинк
Cтраница 1
Восстановление цинка, как полагают, происходит из комплекса и при достаточно высокой катодной поляризации, которая обусловлена как диффузионными ограничениями, так и торможением электрохимической стадии. [1]
Восстановление цинка и кадмия из сернистых руд производят в две стадии. [2]
Восстановление цинка, как полагают, происходит из комплекса и при достаточно высокой катодной поляризации, которая обусловлена как диффузионными ограничениями, так и торможением электрохимической стадии. [3]
Восстановление цинка и кадмия из сернистых руд производят в две стадии. [4]
Процесс восстановления цинка из его окнси ZnO водородом имеет некоторые особенности. Имеются указания 34, что восстановление начинается уже при 310 С. [5]
Потенциал восстановления цинка из цианистого электролита гораздо более отрицательный, чем в случае кислого электролита. [6]
Потенциал восстановления цинка из цианистого электролита гораздо более отрицательный, чем в случае кислого электролита. [7]
Процесс восстановления цинка из его окиси ZnO водородом имеет некоторые особенности. [8]
Другой метод восстановления цинка заключается в электролитическом выделении его из сульфата. Последний получается обработкой обожженных концентратов серной кислотой. [9]
При этом процесс восстановления цинка и железа в основном подчиняется закономерностям восстановления структурно свободных окислов цинка и железа. [10]
Титрование проводят по току восстановления цинка при потенциале - 1 5 в ( Нас. Кривая титрования имеет форму, изображенную на рис. 3 ( см. стр. Титрование можно проводить в присутствии магния, если содержание его не превышает содержание кальция больше чем в пять раз. [11]
 |
Медно-цинковый элемент 2. [12] |
Очевидно, что знак потенциала восстановления цинка противоположен знаку потенциала окисления. Это справедливо для всех электродных реакций. [13]
Например: на фоне хлорида калия потенциалы восстановления цинка и никеля столь близки, что их волны совпадают, в растворе же соли аммония с аммиаком потенциалы полуволн этих элементов отличаются примерно на 400 мв, в таком растворе оба элемента определяются и при совместном присутствии; в) фон определяет границы полярограммы - анион определяет начало волны, катион - конец полярограммы; г) состав и концентрация фона часто влияют на высоту волны. [14]
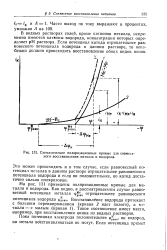 |
Схематические поляризационные кривые для совместного восстановления металла и водорода. [15] |
Страницы: 1 2 3