Восстановление - углекислый газ
Cтраница 3
Выше зоны горения расположена зона восстановления, в которой образовавшаяся в зоне горения двуокись углерода углекислый газ) полностью или частично реагирует с раскаленным углем при температуре 1000 - 1100; при этом происходит восстановление углекислого газа до окиси углерода. [31]
Несомненно, что для восстановления такого прочного окисла, как окись цинка, Ларссону пришлось усиленно работать мехами; жар в его горне был настолько велик, что вслед за реакцией ZnO - - C-i Zn4 - CO2 тотчас же происходило восстановление углекислого газа углем ( который Ларссоном был взят в четверном избытке) в окись углерода. [32]
Восстанови тельная зо-н а. Развита реакция восстановления углекислого газа углеродом с образованием окиси углерода. Происходит расплавление подогретого в четвертой зоне чугуна. [33]
Рассмотренный выше метод синтеза фенил - и фурилкар-бонатов амальгамным способом путем взаимодействия фенола или фурилового спирта с амальгамой щелочного металла и двуокисью углерода, по-видимому, является более простым и удобным, чем чисто химические методы. Образования органических производных угольной кислоты можно также ожидать при проведении процесса восстановления углекислого газа и в других растворителях, содержащих активный атом водорода, например, водород аминогруппы, водород сульфгидрильной группы или водород, активированный соседством какой-нибудь полярной группы. [34]
Анализируя полученные результаты, авторы пришли к выводу, что низкий коэффициент использования тока получается вследствие медленного разложения амальгамы. В 1940 г. Петье [41] получил патент, в котором предлагается проводить процесс восстановления углекислого газа амальгамами щелочных металлов под давлением. [35]
Вода также непосредственно участвует в метаболизме. Она служит источником кислорода, выделяемого в ходе фотосинтеза, и водорода, используемого для восстановления углекислого газа. При образовании АТФ - важного микроэнергетического соединения - из АДФ и фосфата происходит отщепление воды; иными словами, фосфорилирование есть не что иное, как процесс дегидратации, происходящий в водном растворе в биологических условиях. Таким образом, знание многих уникальных свойств воды имеет громадное значение для общего понимания физиологии растений и животных. [36]
Авторами исследования дана зависимость, иллюстрирующая влияние температуры. Чем выше температура, тем больше получается окиси углерода, тем полнее и быстрее протекает процесс восстановления углекислого газа. Показано также влияние реакционной способности различных видов углерода - древесного угля, каменноугольного кокса и антрацита. Скорее всего СО2 восстанавливается углеродом древесного угля; значительно медленнее протекает контакт с каменноугольным коксом и больше всего времени необходимо для восстановления СО2 при взаимодействии с антрацитом. Все эти общие зависимости отвечают практике газификации. [37]
Для того, чтобы хлоропласты могли осуществлять интенсивный фотосинтез вне леток, требуется соблюдение нескольких обязательных условий. Во-первых, необходимо, чтобы при извлечении из клеток не происходило или было минимальным вымывание ферментов, катализирующих реакции фотосинтетического восстановления углекислого газа. [38]
Фотоокислению могут подвергаться молекулы и ионы - органические и неорганические. Роль реакций фотоокисления исключительно велика, так как природный фотосинтез вероятнее всего начинается с фотоокисления воды, сопряженная же темновая реакция - восстановление углекислого газа до углеводов. [39]
По всей вероятности, циклическое фотофосфорилирование является главным источником АТФ для тех биосинтетических процессов в хлоропласта:, которые непосредственно не связаны с восстановлением углекислого газа. [40]
Ларссону пришлось усиленно работать мехами, и жар в его горне был настолько велик, что вслед за реакцией: ZnO - j - С - Zn - f CO2) тотчас же происходило восстановление углекислого газа углем ( который Ларссоном был взят в четверном избытке) э окись углерода. [41]
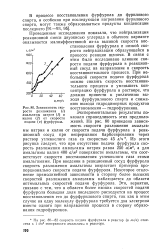 |
Зависимость скорости разложения ( / амальгамы натрия ( / и калия ( 2 от скорости подачи ( о фурфурола. [42] |
Из этого рисунка следует, что при отсутствии подачи фурфурола скорость разложения амальгамы натрия равна 250 а / м2, а для амальгамы калия 400 а / м2 поверхности амальгамы, что соответствует скорости восстановления углекислого газа этими амальгамами. При введении в реакционный сосуд фурфурола скорость разложения амальгамы возрастает примерно пропорционально скорости подачи фурфурола. Некоторое отклонение прямолинейной зависимости в сторону более высоких скоростей разложения амальгамы наблюдается до области оптимальных скоростей подачи фурфурола. Это, вероятно, связано с тем, что в области более низких скоростей подачи фурфурола большая доля последнего расходуется на процесс восстановления его до фурфурилового спирта, так как в этом случае на одну молекулу фурфурола требуется два электрона вместо одного при направлении процесса в сторону образования гидрофуроинов. [43]
Ушер и Пристли [12] утверждали, что хлорофильные пленки на желатине образуют перекись водорода и формальдегид, если их выставлять на свет в присутствии углекислого газа. Но это утверждение, хотя и поддержанное Шрайвером [15], было опровергнуто Юартом [13], Эйлером [14], Шиллером и Бауром [16], Уорнером [17] и Ваге-ром [18], которые показали, что если и можно найти следы формальдегида после освещения хлорофилла на воздухе, то он получается за счет окисления самого хлорофилла, а не восстановления углекислого газа. Вилыптеттер и Штоль [20] установили, что формальдегид вовсе не образуется, если применять чистые хлорофильные препараты. Шода и Швейцер [19] пытались получить формальдегид ж перекись водорода, освещая хлорофилл, осажденный на карбонате кальция, но Вилынтеттеру и Штолю не удалось подтвердить этого. Вильштеттер и Штоль полагали, что хлорофилл содержится в листьях в коллоидальной форме, и потому провели несколько экспериментов по фотосинтетической активности коллоидальных растворов хлорофилла в воде. Результаты были полностью отрицательны. [44]
В литературе есть предположения, что летучесть соединений германия при наличии углекислого газа обусловлена образованием окиси углерода и, возможно, комплексных соединений германия, которые получаются при взаимодействии выделяющихся соединений германия с образующейся окисью углерода. Такой вывод сделан С. Н. Гордон [78] на основании собственных экспериментов, расчетов и анализов результатов работ других исследователей. Наряду с реакцией восстановления углекислого газа с образованием окиси углерода С02 С - - 2СО возможна и реакция прямого взаимодействия соединений германия с двуокисью углерода. Кроме теоретического обоснования, гипотеза подкреплена термодинамическими расчетами. Однако карбонильные соединения германия никем из исследователей не были получены. [45]
Страницы: 1 2 3 4