Восстановление - галогенид
Cтраница 1
 |
Прибор для получения SiI4. [1] |
Восстановление галогенидов или сульфидов происходит с большим трудом, так как склонность водорода соединяться с хлором, бромом, иодом или серой меньше, чем с кислородом. В соответствии с возрастанием сродства к водороду ( HF, H2O, HC1, НВг, H2S, HI) лучше всего восстанавливаются фториды и значительно хуже хлориды. Однако применение галогенидов в большинстве случаев не имеет каких-либо преимуществ; как правило, безводные галогениды получаются из окислов лишь с большим трудом. Галогениды применяют только тогда, когда образование смешанной окисной фазы затрудняет полное восстановление. [2]
Восстановление галогенидов активными металлами ведет к образованию элементарного урана. [3]
Восстановление галогенидов кальцием необходимо проводить при температурах выше точек плавления лантанидов с тем, чтобы обеспечить выплавку металлического слитка. При этом шлак должен находиться в расплавленном состоянии. [4]
Восстановление галогенидов тория до металла, в частности кальцием, рассматривается в разделе 8.4. Металлический торий сохраняет гранецентрированную кубическую структуру вплоть до 1400 С. [5]
Восстановление галогенидов кремния водородом может быть проведено и в присутствии других электроположительных металлов. [6]
Восстановление галогенидов металлов в присутствии дифосфина с образованием нульвалентных производных обсуждается в другом месте ( стр. [7]
При восстановлении галогенидов магнием и алюминием получаются сплавы РЗЭ с восстановителями, причем выход в сплав недостаточно высокий. Магний можно отделить от РЗЭ вакуумной дистилляцией при температуре выше температуры плавления лантанида, но алюминий достаточно полно этим способом не удаляется. [8]
Первая волна восстановления галогенидов во всех фоновых электролитах одноэлектронна и имеет диффузионный характер: зависимость id от ] / Н линейна, температурный коэффициент 0 44 % на 1 С, ток пропорционален концентрации в пределах от 5 35 - 10 - 3 до 2 5 - 10 - 4Af; E /, линейно зависит от концентрации и сдвигается в область отрицательных потенциалов на 0 14 в при увеличении концентрации в указанных пределах. [9]
Различные методы восстановления галогенидов в некоторой степени напоминают процесс Пиджона по восстановлению окиси магния металлическим кремнием, применяемый для получения магния. Процесс восстановления протекает лишь в том случае, когда давление паров получаемого металла при температуре реакции превышает давление паров всех остальных компонентов, участвующих з реакции. Самарий и европий удовлетворяют этим условиям, так как упругость паров их окислов сравнительно невелика. [10]
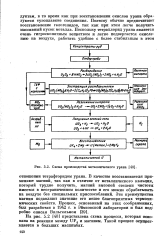 |
Схема производства металлического урана. [11] |
Поэтому обычно предпочитают восстановление галогенидов, так как при этом легче получить массивный кусок металла. [12]
Первая одноэлектронная стадия восстановления галогенидов протекает с разрывом связи Fe - X и образованием радикала [ я - С6Н6Ре ( СО) 2 ]; легкость восстановления увеличивается от - С1 к J. Радикал реагирует с материалом электрода с образованием ртутного соединения, которое восстанавливается до 18-электронного аниона [ я - СвН5Ре ( С0) 2 ] с разрывом связи Fe - Hg в одну двухэлектронную стадию. [13]
Глубина и скорость восстановления галогенидов титана и ванадия значительно различаются. [14]
Лучше всего изучены реакции восстановления галогенидов титана. [15]
Страницы: 1 2 3 4