Восстановление - гидроперекись
Cтраница 2
 |
Концентрация гидроперекис. [16] |
Превращение альдегида в надкисло-ту ( Е) является хорошо известной реакцией; затем надкислота восстанавливается в карболовую кислоту ( F) по реакции, аналогичной восстановлению гидроперекиси до спирта. [17]
Восстановление гидроперекиси водородом над палладиевой чернью дает соответствующий хинол, а разложение в присутствии солей двухвалентного кобальта и исходного фенола приводит к смеси, в которой были идентифицированы указанный выше хинол и продукты димеризации бензильного радикала. [18]
Как видно из данных таблиц, процент восстановления гидроперекиси зависит в основном от концентрации и количества водных растворов восстановителя. Лучшие результаты получены при восстановлении гидроперекиси щелочью, при этом содержание гидроперекиси в оксидатах можно довести до минимума. [19]
 |
Схема установки для концентрирования гидроперекиси. 1 - подогреватель. 2 - капельница. 3 - t - приемник. 5 - холодильник. [20] |
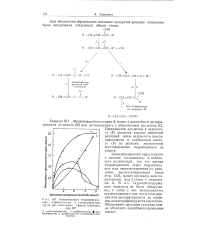
Для восстановления было взято 200 г окисленной фракции тримеров пропилена, содержащей 20 3 % гидроперекисей, и 400 г 10 % - ного водного раствора сульфита натрия, смесь нагревалась при 80 и энергичном перемешивании. На рис. 4 показана скорость восстановления гидроперекисей. Восстановление идет довольно быстро в первые 4 часа, а затем замедляется. Остаток был разрушен обработкой реакционной смеси 10 % - ным водным раствором сернокислого закисцого железа FeS04, и реакционная смесь уже практически не содержала гидроперекиси. [21]
Наиболее часто в качестве отверждающего агента используют гидроперекись кумола. Однако загрязнение полимера образующимся при восстановлении гидроперекиси кумиловым спиртом отражается на пластичности отвержденного продукта. Щелочные добавки ускоряют отверждение при комнатной температуре, поэтому обычно в реакционную смесь вводят небольшие количества органических аминов. Наиболее эффективны добавки три ( диметиламинометил) фенола или алифатических аминов, так как на их действии меньше отражается присутствие влаги, чем на действии дифенилгуанидина, который применялся раньше. [22]
В результате ускоряется разложение полимера. Поэтому роль антиоксиданта должна заключаться также в восстановлении гидроперекиси в более стойкие продукты - спирты ROH. Иногда для этой цели вводят восстановители, например органические сульфиды. [23]
Из приведенных в табл. 1 данных видно, что в зависимости от природы окружающих перекисную связь радикалов потенциалы полуволн гидроперекисей различаются. Следовательно, ненасыщенные алкильные и арильные радикалы облегчают восстановление гидроперекисей, что отвечает и понижению прочности перекисной связи в том же направлении. [24]
Варианты иодометрического метода определения гидроперекиси в водных средах доказывают, что восстановление ее йодистым водородом идет скорее и полнее в гомогенной реакционной смеси. Так, в среде безводной ( ледяной) уксусной кислоты реакция восстановления гидроперекиси HJ протекает с большой скоростью. Концентрация йодистого калия 25 г / л и избыток, равный 1 7-кратному по отношению к теоретически необходимому расходу его, вполне достаточны, чтобы реакция при: 14 - 16 С практически закончилась за 15 - 20 мин. Поскольку при доступе воздуха KJ частично окисляется кислородом, что дает завышенные результаты определения гидроперекиси, реакцию необходимо проводить в атмосфере инертного газа. [25]
Восстановление перекисей позволяет получать спирты, альдегиды и кетоны. Спирты можно получать также восстановлением гидроперекисей, которые синтезируют обычно окислением молекул с третичным атомом углерода ( разд. Восстановление проходит при действии триалкилфосфинов и триалкилфосфитов [ Davies, стр. Часто используют сульфит натрия [ Вег. [26]
Из дналкилбензолов с двумя различными алкильными группами с точки зрения аутоокисления наиболее удобен цимол. Первые исследователи22 считали, что этот углеводород дает первичную гидроперекись, так как при ее разложении в кипящей воде образуется и-изопропилбензальдегид. Последующие же авторы23, изучая продукты восстановления выделенной гидроперекиси, нашли 2-л-толилпропанол - 2 ( 90 %) и / г-метилацетофе-нон ( 10 %), что указывает па наличие только третичной гидроперекиси. Сериф, Хаит и Боурнс24 тщательно изучили продукты окисления - цимола в эмульсии при 85 и 60 С и фотохимического окисления при 60 С и, выделив гидроперекись через натриевую соль, доказали, что она является третичной. Очевидно, отсутствие первичной гидроперекиси в выделенном продукте объясняется ее неустойчивостью. Кроме продуктов разложения двух моногидроперекисей из оксидата была выделена также - ( 2-гидроперокси - 2-пропил) - бензойная кислота, образующаяся из дигидроперекиси. [27]
Из дналкилбензолов с двумя различными алкильными группами с точки зрения аутоокисления наиболее удобен цимол. Первые исследователи22 считали, что этот углеводород дает первичную гидроперекись, так как при ее разложении в кипящей воде образуется и-изопропилбензальдегид. Последующие же авторы23, изучая продукты восстановления выделенной гидроперекиси, нашли 2-л-толилпропанол - 2 ( 90 %) и / г-метилацетофе-нон ( 10 %), что указывает на наличие только третичной гидроперекиси. Сериф, Хаит и Боурнс24 тщательно изучили продукты окисления - цимола в эмульсии при 85 и 60 С и фотохимического окисления при 60 С и, выделив гидроперекись через натриевую соль, доказали, что она является третичной. Очевидно, отсутствие первичной гидроперекиси в выделенном продукте объясняется ее неустойчивостью. Кроме продуктов разложения двух моногидроперекисей из оксидата была выделена также - ( 2-гидроперокси - 2-пропил) - бензойная кислота, образующаяся из дигидроперекиси. [28]
Страницы: 1 2