Азометин
Cтраница 3
О получении азометинов и уротропина и их гидролизе см. разд. [31]
В масс-спектрах азометинов ( бензилиденанилинов) типа RO - С6Н4 - CH N - C6H4 - Ri ( R и R, - алкиль-иые группы) имеются интенсивные пики молекулярных ионов с нечетным значением массы, что естественно для соединений, содержащих один атом азота. Например, пики молекулярных ионов МББА, ЭББА и ПББА являются в спектрах максимальными, и их доля составляет не менее 25 % от полного ионного тока. Молекулярные массы соединений этой группы отличаются на две единицы от молекулярных масс соединений первого типа, что позволяет их легко различать. [32]
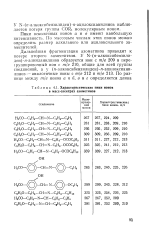 |
Характеристические пики ионов в масс-спектрах азометинов. [33] |
Дальнейшая фрагментация азометинов приводит к потере второго заместителя. [34]
Реакция образования азометинов используется для временной защиты аминогруппы и в качестве промежуточных стадий органического синтеза. [35]
Комплексы таких азометинов с железом, кобальтом, марганцем, медью, никелем и алюминием разлагаются в минеральнокислой красильной ванне. Однако хромовые комплексы о о - диоксидиарил-азометинов в тех же условиях более устойчивы, несмотря на легкость гидролиза исходных азометинов под действием кислоты. Однако красящая способность хромовых комплексов азометинового ряда значительно ниже и они не нашли большого технического применения. [36]
При нагревании азометинов с аминами, амины с большей основностью вытесняют менее основные. При этом устанавливаются равновесия, положение которых определяется соотношением рКь использованных аминов. [37]
Щелочной гидролиз азометинов протекает медленнее, чем кислотный. [38]
Возможность синтеза азометинов, основанного на реакции иминного обмена, обусловлена равновесной природой реакций конденсации аминов с карбонильными соединениями ( ср. Так, анилы R2C NAr реагируют с гидроксиламином или гидразинами и дают в результате иминного обмена соответствующие оксимы и гидразоны; в свою очередь, при реакции ок-симов с гидразинами получают гидразоны. Равновесие часто можно сместить в нужном направлении, особенно если аминный компонент, подлежащий замещению, более летуч, чем вновь вступающий. Это превращение особенно целесообразно применять в случае иминов, являющихся производными затрудненных кето-нов, которые заведомо с трудом будут вступать в непосредственную конденсацию. [39]
У четвертичных солей азометинов азот CHN-группы кватер-низован. Это существенно увеличивает энергию пя - состояния. Можно предположить, что Т - уровень оказывается выше5я - уровня. Тогда резко снижается вероятность интеркомбинационной конверсии и возникает флуоресценция. [41]
Спектры поглощения всех азометинов измерены в дихлорэтане. По мере увеличения числа конденсированных бензольных колец в альдегидной части молекулы интенсивность этой полосы растет, причем у 9-антральанилина она смещена батохром-но по сравнению с бензаль - и 1-нафтальанилинами. [42]
Изучение полярографического поведения азометинов, имеющих строение n - XC6H4CH NC6H5 и C6H5CH NC6H4Y - ( где X и Y - различные заместители), в ДМФ показало [16-19], что суммарный электродный процесс характеризуется присоединением к молекуле деполяризатора двух электронов и контролируется в основном диффузией его к электроду. [43]
Изучение полярографического поведения азометинов, имеющих строение n - XC6H4CHNC6H5 и C6H5CH NC6H4Y - n ( где X и Y - различные заместители), в ДМФ показало [16-19], что суммарный электродный процесс характеризуется присоединением к молекуле деполяризатора двух электронов и контролируется в основном диффузией его к электроду. [44]
Нитроны ( N-оксиды азометинов) под ЭУ способны изомеризоваться в оксазираны. Поэтому в масс-спектрах таких соединений присутствуют пики, обусловленные обеими формами. [45]
Страницы: 1 2 3 4
