Число - колебательная степень - свобода
Cтраница 3
Многоатомная молекула может совершать большое число колебательных движений, равное числу колебательных степеней свободы. Это число подсчитывается следующим образом. Молекула из N атомов имеет 3N степеней свободы. Три из них приходятся на координаты центра инерции молекулы. Число вращательных степеней свободы в общем случае также равно трем. Однако у линейных молекул всего лишь две вращательные степени свободы, поскольку вращение около линии, проходящей через центры атомов, лишено физического содержания. Как бы то ни было, число колебательных частот, а значит, и число полос в инфракрасном спектре, строго определено числом атомов и симметрией молекулы. [31]
Зп - общее число степеней свободы молекулы; / кол - число колебательных степеней свободы, равное Зп - 6 для нелинейной молекулы и Зп - 5 для линейной. Выражения (IV.83) - (IV.85) представляют собой запись закона равнораспределения энергии. [32]
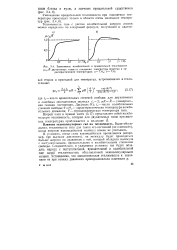 |
Зависимость колебательной и вращательной теплоемкости двухатомных газов от отношения температуры вещества к характеристическим температурам. а - Tlfv. б - T / Qr. [33] |
Дж / ( моль - К); г, - число колебательных степеней свободы; 0 6 - характеристическая температура колебательного движения; Т - термодинамическая температура газа. [34]
Мольная теплоемкость газа значительно возрастает с усложнением его молекулы вследствие увеличения числа колебательных степеней свободы. Поэтому органические соединения с многоатомными молекулами трудно нагреть до высокой температуры адиабатическим сжатием. [35]
В случае газов молекулы можно рассматривать как отдельные частицы, для которых число колебательных степеней свободы невелико: оно составляет ( 3 - 5) в линейных и ( 3 - 6) в нелинейных молекулах. [36]
Здесь нужно только указать, что в связи с определением конфигурации и числа колебательных степеней свободы активированной молекулы возникает необходимость учета возможности внутреннего вращения последней. [37]
Существенное отличие активированного комплекса от обычных молекул состоит также в том, что число колебательных степеней свободы в переходном состоянии меньше на единицу - отсутствует колебательное движение по направлению так называемой реакционной координаты, вдоль пути реакции. Это различие очень важно в количественных расчетах, основанных на методе переходного состояния. [38]
В сложных молекулах появление внутренних вращательных степеней свободы связано с исчезновением такого же числа колебательных степеней свободы. [39]
В 1927 г. Гиншелвуд [3] предположил, что скорость возбуждения молекулы зависит от числа колебательных степеней свободы в ней. Молекула с большим числом колебательных степеней свободы имеет гораздо больше шансов приобрести необходимую для активации энергию, так как эта энергия может распределяться между всеми степенями свободы. [40]
Отличие, связанное с атомной структурой вещества, проявляется только в том, что число колебательных степеней свободы должно оставаться равным 3jV, а не являться бесконечным. [41]
Так же, как в случае газовых реакций, константа скорости мономолекулярных реакций в растворах зависит от числа колебательных степеней свободы ( внутренних колебаний) S. Если ERT, то доля активных молекул, а следовательно, и константа скорости реакции, падает с ростом числа степеней свободы внутренних колебаний. Однако с такими реакциями в кинетике почти не приходится встречаться. [42]
 |
Внутреннее вращение в В заключение можно добавить, что молекуле этана. ПрИ ВЬ1ЧИСЛеНияХ, связанных С ХИМИ. [43] |
Возможность внутреннего вращения должна учитываться при составлении полной суммы по состояниям - она в первую очередь уменьшает число колебательных степеней свободы. [44]
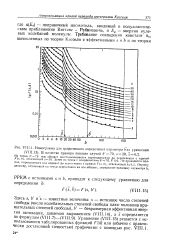 |
Номограмма для графического определения параметра b из уравнения. [45] |
Страницы: 1 2 3 4