Время - жизнь - возбужденное состояние
Cтраница 1
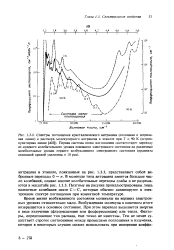
Время жизни возбужденного состояния в отсутствие химических превращений с его участием определяется суммой рассмотренных процессов физической дезактивации. Из возбужденных состояний наиболее долгоживущим является состояние Гь на превращение которого в состояние S0 наложен запрет по спину. В связи с этим легче осуществляется и чаще применяется в фотохимии Т-7-перенос энергии, и увеличивается, сравнительно с Si-состоянием, вероятность участия в химической реакции состояния TI. В случае, если возбужденная молекула подвергается химическому превращению ( химическая дезактивация), время жизни возбужденного реакционноспособного состояния становится меньше, чем в отсутствие реакции, и определяется всей совокупностью процессов физической и химической дезактивации. Очевидно, эффективность фотохимической реакции зависит от конкуренции химического процесса с процессами физической дезактивации. Рассмотренные представления о возбуждении молекул и их физической и химической дезактивации поясняет схема а рис. 23, которая упрощена, так как на ней не показаны колебательные уровни каждого из электронных состояний. [1]
Время жизни возбужденного состояния по отношению к испусканию света часто можно определять в терминах кинетики процесса первого порядка. Если испускание является единственным способом рассеивания энергии возбужденного состояния, то величина, обратная константе скорости исчезновения этого состояния, называется естественным временем жизни т возбужденного состояния. [2]
Времена жизни возбужденных состояний с т - 1 и - 1, очевидно, одинаковы. [3]
Время жизни возбужденного состояния или реакционноспособ-ных частиц является одним из основных факторов, определяющих течение фотореакции. Для состояний с относительно большим временем жизни вероятность их фотохимического превращения превышает вероятность процесса дезактивации в основное состояние путем безызлучательных переходов или излучения света. Обычно естественное время жизни возбужденного состояния или реакционных частиц т ( в секундах) определяется как время, за которое концентрация возбужденных молекул падает до 1 / е от первоначальной. [4]
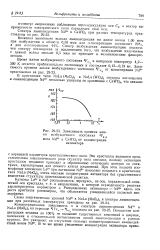 |
Зависимость времени жизни возбужденного состояния 4F3 / J. [5] |
Время жизни возбужденного состояния 4F3 / 2 в интервале температур 4 2 - 300 К остается приблизительно постоянным и составляет 0 12 - 0 19 мс. [6]
Время жизни возбужденных состояний определяется главным бразом двумя механизмами: стимулированным процессом испус-ания и спонтанным процессом испускания. [7]
Времена жизни возбужденных состояний ( в секундах) для кон-денсированных ( жидких) систем показаны на следующей схеме. [8]
Время жизни возбужденного состояния определяется как время, за которое первоначальное количество возбужденных состояний уменьшается в е раз. [9]
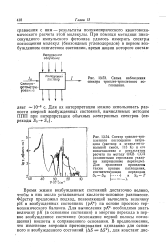 |
Схема наблюдения спектра триплет-триплетного поглощения. [10] |
Время жизни возбужденных состояний достаточно велико, чтобы в них могло установиться кислотно-основное равновесие. Ферстер предложил подход, позволяющий вычислять величину рН в возбужденных состояниях ( рД) на основе простого термохимического баланса. Для вычисления рК необходимо знать величину р / ( ( в основном состоянии) и энергию перехода в первое возбужденное состояние ( положение первой полосы поглощения) кислоты и сопряженного основания. [11]
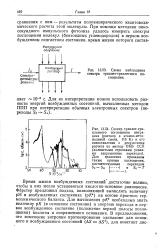 |
Схема наблюдения спектра триплет-триплетного поглощения. [12] |
Время жизни возбужденных состояний достаточно велико, чтобы в них могло установиться кислотно-основное равновесие. Ферстер предложил подход, позволяющий вычислять величину рН в возбужденных состояниях ( рК) на основе простого термохимического баланса. Для вычисления р / С необходимо знать величину рК ( в основном состоянии) и энергию перехода в первое возбужденное состояние ( положение первой полосы поглощения) кислоты и сопряженного основания. [13]
Время жизни возбужденного состояния молекулы на верхних электронных уровнях относительно мало. Возбужденная молекула в конечном итоге возвращается в основное состояние. При этом переходе выделяется энергия в виде излучения ( флуоресценция или фосфоресценция) или тепла. Факторы, определяющие тип распада, еще точно не известны. [15]
Страницы: 1 2 3 4 5