Время - молекула
Cтраница 2
В то же время молекулы растворенного вещества могут изменить ориентацию молекул воды, вследствие чего значение AS может стать отрицательным. Если растворяемое соединение является твердым веществом, изменение пространственной энтропии для его растворения будет положительным; при растворении газа изменение пространственной энтропии отрицательно; если же растворяемое соединение является жидкостью, изменение пространственной энтропии должно приближаться к нулю. Если силы притяжения между молекулами растворенного вещества и молекулами воды больше, чем средняя величина из сил притяжения между молекулами воды и сил притяжения между молекулами растворяемого вещества, то величина А / / для процесса растворения будет отрицательной ( что способствует повышению растворимости), и наоборот. [16]
В то же время молекулы растворенного вещества могут изменить ориентацию молекул воды, вследствие чего значение AS может стать отрицательным. Если растворяемое соединение является твердым веществом, изменение пространственной энтропии для его растворения будет положительным; при растворении газа изменение пространственной энтропии отрицательно; если же растворяемое соединение является жидкостью, изменение пространственной энтропии должно приближаться к нулю. Если силы притяжения между молекулами растворенного вещества и молекулами воды больше, чем средняя величина из сил притяжения между молекулами воды и сил притяжения между молекулами растворяемого вещества, то величина ДЯ для процесса растворения будет отрицательной ( что способствует повышению растворимости), и наоборот. [17]
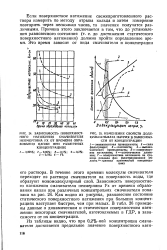
В течение этого времени молекулы смачивателя переходят из раствора смачивателя на поверхность воды, где образуют мономолекулярный слой. Как видно из рисунка, равновесное состояние статического поверхностного натяжения при больших концентрациях наступает быстрее, чем при малых. В табл. 26 приведены данные о динамическом и статическом поверхностном натяжении некоторых смачивателей, изготовляемых в ГДР, в зависимости от их концентрации. [19]
В начальный момент времени N молекул равновесного идеального газа занимают при температуре Т сферический объем радиуса R. Затем газ начинает беспрепятственно расширяться в пустоту. [20]
Количество активирующихся в единицу времени молекул во много раз превышает количество молекул, которые претерпевают химическое превращение, но подавляющее большинство их дезактивируется, не успев прореагировать. Это возможно тогда, когда время жизни активированных молекул велико, и для реакции необходимо перераспределение энергии по связям внутри активированных молекул. Перераспределение происходит после активирующего столкновения. Подобные реакции наблюдаются у молекул сложного строения, состоящих из большого числа атомов. [21]
За самый короткий промежуток времени молекулы газа даже при давлении - 10 - 17 мм рт. ст. совершают большое число столкновений с молекулами стенок сосуда. [22]
Количество ионизируемых в единицу времени молекул протекающего газа, а следовательно, и ионизационный ток являются функцией состава газовой среды. [23]
На какую величину - tm ( межкаталитическое время молекулы фермента) или tk ( каталитическое время молекулы фермента) - и как влияют аналоги субстратов. Одинаково ли это влияние при разных концентрациях субстрата. [24]
При химическом равновесии число образующихся в единицу времени молекул ( или других частиц) при прямой реакции равно числу молекул ( других частиц), вступивших во взаимодействие при обратной реакции, т.е. химическое равновесие является динамическим. В состоянии химического равновесия скорость прямой реакции равна скорости обратной реакции. [25]
Во сколько раз уменьшится число столкновений г в единицу времени молекул двухатомного газа, если объем газа адиабатически увеличить в - 2 раза. [26]
Сочетание масс-спектрометрической методики и метода молекулярного пучка полезно при исследовании времени жизггя молекул в адсорбированном состоянии на поверхности. [27]
Скорость химической реакции ( измеряемая, скажем, числом прореагировавших в единицу времени молекул) зависит от температуры газовой смеси, в которой она происходит, увеличиваясь вместе с ней. Скорость реакции может при этом оказаться при обычных температурах настолько малой, что реакция практически вовсе не идет, несмотря на то, что состоянию термодинамического ( химического) равновесия соответствовала бы газовая смесь, компоненты которой прореагировали друг с другом. При достаточном же повышении температуры реакция протекает со значительной скоростью. Если реакция эндотермична, то для ее протекания необходим непрерывный подвод тепла извне; если ограничиться одним только начальным повышением температуры смеси, то прореагирует лишь незначительное количество вещества, вслед за чем температура газа настолько понизится, что реакция снова прекратится. [28]
Скорость химической реакции ( измеряемая, скажем, числом прореагировавших в единицу времени молекул) зависит от температуры газовой смеси, в которой она происходит, увеличиваясь вместе с ней. Скорость реакции может при этом оказаться при обычных температурах настолько малой, что реакция практически возсе не идет, несмотря на то, что состоянию термодинамического ( химического) равновесия соответствовала бы газовая смесь, компоненты которой прореагировали друг с другом. При достаточном же повышении температуры реакция протекает со значительной скоростью. Если реакция эндотермична, то для ее протекания необходим непрерывный подвод тепла извне; если ограничиться одним только начальным повышением температуры смеси, то прореагирует лишь незначительное количество вещества, вслед за чем температура газа настолько понизится, что реакция снова прекратится. [29]
На какую величину - tm ( межкаталитическое время молекулы фермента) или tk ( каталитическое время молекулы фермента) - и как влияют аналоги субстратов. Одинаково ли это влияние при разных концентрациях субстрата. [30]
Страницы: 1 2 3 4