Время - полупревращение
Cтраница 1
Время полупревращения - это время, за которое начальная концентрация уменьшается наполовину. [1]
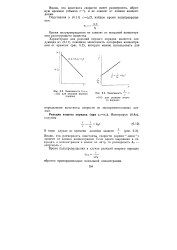 |
Зависимость In c.| Зависимость - с. [2] |
Время полупревращения не зависит от исходной концентрации реагирующего вещества. [3]
 |
Накидная гайка из эбонита. [4] |
Время полупревращения эталонного изопрена в растворе эталонного изопентана при загрузке катализатора 0 5 % ( масс.) [ из расчета на хлорид титана ( IV) ] должно быть не более 15 мин. [5]
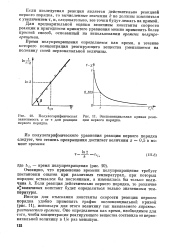 |
Полулогарифмическая зависимость ж от т для реакции первого порядка.| Экспоненциальная кривая реакции первого порядка. [6] |
Время полупревращения определяется как время, в течение которого концентрация реагирующего вещества уменьшается на половину своей первоначальной величины. [7]
 |
График зависимости х / а ( а - х от времени для реакции второго порядка. [8] |
Время полупревращения снова обратно пропорционально k, однако здесь в отличие от реакции первого порядка, где т не зависит от а, оно обратно пропорционально а. Такой результат всегда указывает на то, что имеет место реакция второго порядка. [9]
Время полупревращения веществ в реакции 1-го порядка при 323 К составляет 100 мин, а при 353 К - 15 мин. [10]
Время полупревращения катион-радикала, по данным циклической вольтамперометрии, составляет около 5 с. При воспроизведении циклических вольтамперо-грамм в ацетонитриле появляются два новых пика окисления. [11]
Время полупревращения реакции есть время, в течение которого концентрация А уменьшается наполовину по сравнению с начальным значением. [12]
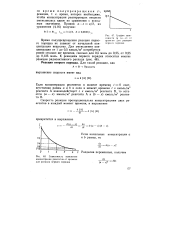 |
График зависимости lg ( a - х от времени для реакции первого порядка.| Зависимость изменения концентрации реагентов от времени для реакции первого порядка. [13] |
Время полупревращения реакции первого порядка не зависит от начальной концентрации вещества. Для уменьшения концентрации от 1 до 0 5 кмоль / м3 потребуется ровно столько же времени, сколько для 0 5 моль до 0 25, от 0 25 др 0 125 моль. [14]
Если время полупревращения изменяется ( график не выражается прямой линией), то скорость реакции зависит от концентрации, но не прямо пропорциональна ей. [15]
Страницы: 1 2 3 4