Пиррольный азот
Cтраница 1
Следовательно, пиррольный азот является более электроотрицательным. При переходе от этих катионов к нейтральным молекулам различие в электроотрицательности атомов азота частично компенсируется большей я-электронной плотностью у пиррольного азота, но недавние неэмпирические расчеты показали, что в пирроле ку-лоновский интеграл для атома азота, вероятно, должен все-таки быть значительно более отрицательным, чем в пиридине. [1]
Электронная пара пиррольного азота уже не имеет свойств свободной электронной пары, которой обусловлена основность аминов и пиридина, а участвует в образовании электронного секстета. [2]
Электронная пара пиррольного азота уже не имеет свойств-свободной электронной пары, которой обусловлена основность аминов и пиридина, а участвует в образовании электронного секстета. [3]
Электронная пара пиррольного азота уже не имеет свойств сво бодной электронной пары, которой обусловлена основность аминов-л пиридина, а участвует в образовании электронного секстета. [4]
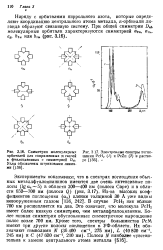 |
Симметрия орбиталей для сопря в фталоцианииах с. [5] |
Наряду с орбиталями пиррольного азота, которые определяют координацию центрального атома металла, я-орбитали ли-ганда образуют связанную систему. [6]
Полагают, что столь высокий мицеллярно-каталити-ческий эффект связан с определенной локализацией и ориентацией протопорфиринового эфира в мицеллах: атомы пиррольного азота локализуются в слое Штерна в непосредственной близости от электростатически связанных ионов меди. [7]
Эти авторы показали, что вещества индольного характера способны хроматографироваться на полиамиде за счет образования водородной связи между атомом водорода пиррольного азота и амидноп группой полиамида. [8]
Опыт показал, что действительно получается не исходный метил-гармин, а изомерное с ним вещество, в котором метильная группа связана с пиррольным азотом. Таким образом, этот опыт тоже гаворит в пользу идеи Перкива и Робинсона о том, что в диалкильных производных гармина обе метальные группы связаны с разными атомами азота. [9]
Проблема С-протонирования имеет прямое отношение к вопросам, связанным с электрофильным замещением и будет подробнее обсуждаться в следующей главе. Сейчас же нас интересует вопрос, возможно ли Л - протонирование пиррольного азота. Величины р / Са карбазола и 9-метилкарбазола в системе H2SO4 - C2H5OH ( 4: 1) равны - 6 0 и - 8 2, соответственно. Это единственная известная в настоящее время количественная информация об основности пиррольного атома азота. [10]
Во всяком случае мы считаем, что в этом вопросе последнее слово еще не сказано. Окончательное доказательство того, что вторая алкиль-ная группа у диалкилгарминов стоит у пиррольного азота, могло бы быть получено или путем изучения производных тетрагидрогармина, или же путем исследования синтетических оснований, в которых эта группа заведомо стоит в указанном положении. [11]
Тетразолы могут отвечать 1Я - ( 21) или 2Я - ( 22) формам. Обе молекулы планарны и ароматичны; секстет составляют один электрон от атома углерода, два от пиррольного азота и по одному от каждого из пиридиновых атомов азота. [12]
Тетразолы могут отвечать Н - ( 21) или 2Н - ( 22) формам. Обе молекулы планарны и ароматичны; секстет составляют один электрон от атома углерода, два от пиррольного азота и по одному от каждого из пиридиновых атомов азота. [13]
Следовательно, пиррольный азот является более электроотрицательным. При переходе от этих катионов к нейтральным молекулам различие в электроотрицательности атомов азота частично компенсируется большей я-электронной плотностью у пиррольного азота, но недавние неэмпирические расчеты показали, что в пирроле ку-лоновский интеграл для атома азота, вероятно, должен все-таки быть значительно более отрицательным, чем в пиридине. [14]
Имидазол является структурным изомером пиразола и по химическим свойствам имидазолы очень схожи с пиразолами. Правда, увеличение расстояния между двумя атомами азота в цикле имидазолов по сравнению с таковым в пиразолах обусловливает более высокую основность имидазола вследствие меньшего влияния пиррольного азота на центр основности. [15]
Страницы: 1 2