Интенсивность - взаимодействие
Cтраница 1
Интенсивность взаимодействия между молекулами монослоя и молекулами соединений, находящихся в подложке, может изменяться в очень широких пределах. [1]
Интенсивность взаимодействия характеризуется постоянной тонкой структуры ( стр. Соответствующие процессы называются электромагнитными и протекают за времена порядка КГ18 - 1СИ7 сек. [2]
Интенсивность взаимодействия с водой значительно увеличивает ся в ряду Li - Cs; Rb и Cs реагируют с водой со взрывом. [3]
Интенсивность взаимодействия между молекулами спирта и воды зависит от концентрации спирта в растворе, давления, температуры, что и обусловливает своеобразие изменения физических свойств растворов с изменением их концентрации. [4]
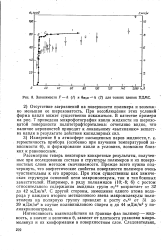 |
Зависимости F - h ( 1 я вщо - Л ( 2 для тонких пленок ПДМС. [5] |
Интенсивность взаимодействия на границе фаз полимер - жидкость, а значит и величина в, зависят от плотности упаковки макромолекул и их конформации в поверхностном слое. [6]
Интенсивность взаимодействия принято характеризовать с помощью так называемой константы взаимодействия, которая представляет собой безразмерный параметр, определяющий вероятность процессов, обусловленных данным видом взаимодействия. Отношение значений констант дает относительную интенсивность соответствующих взаимодействий. [7]
Интенсивность взаимодействия с озоном определяется реакционной способностью эластомера. [8]
Интенсивность взаимодействия с водой значительно увеличивается в ряду Li - Cs; реакция с водой Rb и Cs протекает со взрывом. [9]
Интенсивность взаимодействия с галоидами углеводородов парафинового и нафтенового ряда в значительной мере связана со структурой углеводородных молекул, в частности, с наличием в молекуле водорода при третичном углеродном атоме. Это четко проявляется в реакциях со SbCls. Нормальные парафины, нафтены без боковых цепей и изопарафииы с четвертичным углеродным атомом хлорируются с помощью пятихлористой сурьмы при комнатной температуре очень медленно. Напротив, изопарафины и нафтены с боковыми цепями, обладающие водородом у третичного атома С, хлорируются SbCl5 даже при 0 с большой скоростью. [10]
Интенсивность взаимодействия с водой значительно увеличивает ся в ряду Li - Cs; Rb и Cs реагируют с водой со взрывом. [11]
 |
Схема донорно-акцепторного ( а и дативного ( б механизма образования it - связи.| Влияние а - и к-взаимодействия L - - M и M-L на величину Д. [12] |
Интенсивность взаимодействия a -, я - и яразр-орбиталей лиганда с d - орбиталями центрального атома определяет величину параметра расщепления Д ( см. стр. Как указывалось, чем прочнее а - связь L - М, тем выше уровень aJJa3p - MO, а следовательно, выше значение Д ( см. стр. Аналогичным образом при сильном я - взаимодействии L - - М повышается уровень it ( d) - MO, т.е. вели чина Д уменьшается. [13]
Интенсивность взаимодействия уменьшается при переходе от GeO. [14]
Интенсивность взаимодействия с водой значительно увеличивается в ряду U-Ci; реакция с водой Rb и Се протекает со взрывом. [15]
Страницы: 1 2 3 4