Дифенилфульвен
Cтраница 1
Исходный дифенилфульвен получался, согласно указаниям Тиле [13] путем конденсации циклопентадиена с бензофеноном в присутствии алко-голята натрия в спиртовой среде. [1]
Гидрогенизация дифенилфульвена на скелетном никеле протекала так, что первая молекула водорода присоединялась неселективно. [2]
Гидрогенизация дифенилфульвена проводилась в утке, погруженной в ванну с постоянной температурой и прикрепленной к горизонтально двигающемуся взад и вперед стержню. [3]
Каталитическое гидрирование дифенилфульвена протекает последовательно: сначала две молекулы водорода присоединяются к двум двойным связям цикла без ясно выраженной селективности, а затем очень медленно гидрируется семициклическая двойная связь. [4]
Особенностью строения дифенилфульвена является наличие двух фе-нильных групп у углерода, примыкающего к семициклической двойной связи: быть может, именно этим и объясняется та медленность, с которой водород, под влиянием катализатора, к ней присоединяется. Если это так, то замена фенильных радикалов другими группами, например ме-тильными, должна была бы повлиять на характер присоединения водорода к соответствующему фульвену. [5]
Реакция гидрирования дифенилфульвена на скелетном никеле, судя по исследованию продуктов неполного гидрирования, идет столь же селективно, как и на палладии. [6]
Кинетическая кривая гидрирования дифенилфульвена па скелетном никеле отличается от кривых гидрирования его на платине и палладии. [7]
Эти данные показывают, что дифенилфульвен в диеновом синтезе ведет себя аналогично самому циклопентадиену, и, несмотря на наличие в нем семи-циклической двойной связи, обладает пространственной направленностью аддуктообразования. [8]
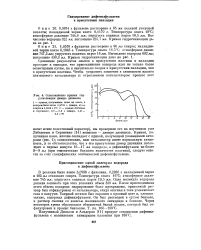 |
Сопоставление кривых гидрогенизации дилера дивинила. [9] |
Полученный Дильсом и Альдером [11] продукт соединения дифенилфульвена с малеиновым ангидридом плавился при 168 С. [10]
Таким образом, в реакции каталитического гидрирования дифенилфульвена можно ясно различить две стадии: присоединение водорода к двойным связям кольца и последующее гидрирование внециклической двойной связи. [11]
По-видимому, это объясняется тем, что наличие двух фенильных групп в молекуле дифенилфульвена вызывает снижение электронной плотности у семициклической двойной связи, благодаря чему уменьшается аккумуляция ненасыщенности по этой двойной связи, и ориентирование по схеме А становится предпочтительным. [12]
В 1936 г. Казанский, Платэ и Гнатенко3 гидрировали диметил -, метилэтил -, диэтил - и дифенилфульвены в различных условиях и получали углеводороды с выходами, не превышающими 50 % от теоретич. [13]
Легко синтезируемый из дпбензоилферроцена и фенилмагнийбро-мида третичный диол в уксусной кислоте с добавкой соляной кислоты легко фотолизуется, количественно превращаясь в дифенилфульвен. Интересно, что резонансный карбониево-аммонийный катион, образующийся в кислой среде из соответствующего карбинола, легко фотолизуется и образует / г-диметиламинофенил-ферроценилфульвен. [14]
Таким образом, присоединение первых двух молекул водорода к диметилфульвену происходит не избирательно, и, следовательно, несмотря на одинаковое строение обоих фульвенов, особый характер гидрирования дифенилфульвена обусловливается ароматической природой заместителей у углерода с семициклической двойной связью. [15]
Страницы: 1 2