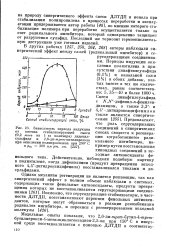
Дифенохинон
Cтраница 1
Дифенохинон, у которого ненасыщенная сопряженная хиноидная система включает оба кольца, имеет очень высокий потенциал и является сильным окислителем. [1]
Дифенохинон, хинон дифенилового ряда, получается при окислении п / г-диоксидифе-нила; он образует желтые иглы. [2]
Дифенохинон восстанавливается также и с помощью солянокислого гидроксиламина в водно-спиртовом растворе. [3]
Миграция дифенохинона, пиридина и формальдегида не была обнаружена во всех случаях. [4]
Как видно из схемы, дифенохинон образуется в результате ди-меризации как промежуточного карбена, так и 2 6-ди-трег - бутил-феноксила с последующим дегидрированием дифенильного производного. В свою очередь, 2 6-ди-грет - бутилфеноксил способен дегидрировать как амины, используемые в качестве среды, так и возникающие фенолы, давая 2 6-ди-грег - бутилфенол. Кроме того, этот феноксильный радикал может рекомбинировать с аминным радикалом ( - NR2) с образованием 4 - Ы М - диалкиламино-2 6-ди-трет - бу-тилфенола. Последний при дегидрировании карбеном или фенокси - лом в присутствии кислорода превращается ( через соответствующую перекись хинолидного типа) в 2 6-ди-грег - бутилбензохи-нон. [5]
Не отмечено также выделение в воду дифенохинона, пиридина и формальдегида. [6]
Действительно, наблюдали подобную картину в полиэтилене, когда дифенохинон ( продукт превращения исходного 4 4 -дигидроксидифенила) восстанавливался тиолами и дисульфидами. [8]
Дальнейшее окисление хинолидного димера, или его таутомерией формы - дигидроксибифенила - приводит к образованию дифенохинона. [9]
Дифенилэтаноламин 393, 406, 624 1 2 - Дифенилэтилендиамин 391 Дифеновые кислоты 162 Дифеновые соединения 455 Дифенохинон 53 Дихинолилы 628 ел. [10]
Такие продукты, как дидодецилдисульфид или додекандитиол-1 10, являются весьма слабыми антиоксидантами, в смеси же с сажей [258], а также с дифенохиноном и полиаценами [266] они значительно уменьшают скорость термоокисления полиэтилена. [11]
Однако в большинстве случаев при наличии заместителей в пара-положении феноксила реакция не останавливается на этой стадии, так как происходит отщепление этих заместителей с образованием дифенохинона. Первый случай подобной димери-зации был отмечен Куком91 на примере поведения радикала из 4-нитро - 2 6-ди-трег - бутилфенола. [12]
Если окислительно-восстановительный потенциал слишком велик, то степень окисления H2S будет чрезмерной и сера не образуется, или катализатор превращается в нежелательное вещество; например, бензохинон или дифенохинон частично превращается в фуминовую кислоту. [13]
Если две различны реакции окисления или восстановления протекают параллельно, то реакция приводится только в одном месте; так, например, получение церулигн-она окислением димети-лового эфира пирогаллола приведено в главе Образование связей между атомами углерода путем окисления, так как первичным процессом в данном случае является возникновение связи между атомами углерода, а окисление в дифенохинон - процессом последующим и так как кроме того в той же главе описывается ряд аналогичных реакций первого типа. Таким образом, если в реакцию могут вступать различные части молекулы, а установить с полной определенностью, какая реакция начнется раньше, невозможно, следует просмотреть несколько глав. [14]
При гидролизе вещества А препаратом танназы из Aspergillus niger образуются последовательно вещества В ж С ( Roberts, Myers, 1959b), что является одним из доказательств приводимой структуры. Другим путем дальнейшего превращения дифенохинонов является их окисление, приводящее к образованию бензотрополо-вого фрагмента. [15]
Страницы: 1 2