Выделение - кадмий
Cтраница 3
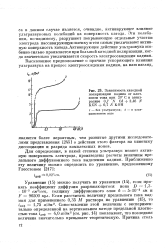 |
Зависимость катодной поляризации кадмия от плотности тока при 20 С в электролите 0 7 N СА 2 46 N KCN 0 7 N КОН. [31] |
Для определения, в какой степени ультразвук меняет активную поверхность электрода, произведены расчеты величины предельного диффузионного тока выделения кадмия. [32]
Препарат, содержащий кадмий - 117т и продукт его распада индий - 117т, через 1 9 ч после выделения кадмия имеет активность 103 имп / мин. [33]
Навеску породы разлагают смесью плавиковой и хлорной кислот и аммиачно-цитратный раствор остатка экстрагируют раствором дитизона в четыреххлористом углероде для выделения кадмия, цинка, свинца, меди и других металлов. Раствор четыреххлористого углерода встряхивают с очень разбавленной соляной кислотой, чтобы перевести кадмий, цинк и другие элементы в водную фазу; медь и кобальт остаются в четыреххлористом углероде. [34]
Важной характеристикой электролиза при контролируемом потенциале-является изменение тока во времени. Рассмотрим выделение кадмия на платиновом катоде из хорошо перемешиваемого 0 01 М раствора Cd ( NH3) 4 I F по аммиаку. [35]
Скорость выделения кадмия на стали может быть повышена до 7 - 8 мкм / ч при использовании многокомпонентного раствора, содержащего ( моль / л): 0 065 CdCi2, 0 195 трилона Б, 0 56 сегнетовой соли, 0 004 ( NH4) 2SO4, 6 4 NaOH, 0 228 NaH2PO2, рН 10; / 100 - г - 110 С, удельная плотность загрузки деталей в ванну 2 дм2 / л [ 141, с. В указанных растворах формируются плотные, но тонкие кадмиевые покрытия, прочно сцепленные с металлом основы. [36]
Раствор подкисляют несколькими каплями H2S04 и ведут электролиз при напряжении 3 - 4 В и катодной плотности тока 0 01 А / см. 2 Электролит часто перемешивают, следя за тем, чтобы рыхлый осадок Cd не вызвал короткого замыкания между электродами. По мере выделения кадмия его извлекают, промывают водой и сплавляют. Для сплавления кадмий помещают в фарфоровый тигель или чашку, нагревают до плавления, затем выливают по каплям в воду ( если хотят получить гранулы) или на чистую стальную поверхность и оставляют до затвердения. [37]
Раствор подкисляют несколькими каплями H2SO4 и ведут электролиз при напряжении 3 - 4 В и катодной плотности тока 0 01 А / см. 2 Электролит часто перемешивают, следя за тем, чтобы рыхлый осадок Cd не вызвал короткого замыкания между электродами. По мере выделения кадмия его извлекают, промывают водой и сплавляют. Для сплавления кадмий помещают в фарфоровый тигель или чашку, нагревают до плавления, затем выливают по каплям в воду ( если хотят получить гранулы) или на чистую стальную поверхность и оставляют до затвердения. [38]
Даниэля; выделением кадмия из р-ррв цинком ( цементация) широко пользуются при получении кадмия. [39]
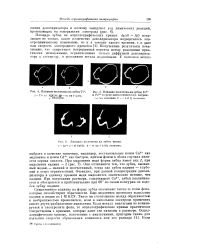 |
Влияние желатины на зубец Т1.| Влияние желатины на зубцы Fe2 и Fe3 в среде щавелевокислого натрия. [40] |
Существенное влияние на форму зубца оказывают также те ионы фона, которые способствуют обратимости. Еще медленнее протекает выделение кадмия и индия из 1 М KGN. Такое же соотношение между обратимостью и необратимостью проявляется, если в капельном электроде применить вместо ртути разбавленные амальгамы. Если металл амальгамы не ионизируется в электролите фона, то осциллографические кривые практически тождественны с кривыми, которые дают эти катионы в растворе. [41]
Если вновь погрузившаяся в раствор поверхность электрода осталась чистой, то, не выключая тока, опускают сосуд с электролитом и сразу же хорошо промывают катод водой [ 635, стр. Для проверки полноты выделения кадмия электролит насыщают сероводородом; желтое окрашивание жидкости показывает, что в растворе остались лишь его следы, образование желтого осадка свидетельствует о недостаточно полном выделении [ 82, стр. [42]
Речь идет о выделении кадмия из смеси продуктов деления или отщепления. Хрома-тографическое выделение с помощью анионита за один цикл позволяло получить кадмий с теми же коэффициентами очистки, но с меньшим выходом ( 62 %) и, конечно, требовало значительно больше времени. [43]
В отличие от цинка кадмий не амфотерен и в щелочи не растворяется и не образует растворимых комплексов в избытке щелочи. Благодаря прочности комплексного соединения потенциал выделения кадмия сильно сдвинут в сторону электроотрицательных значений по сравнению с потенциалом в кислом электролите; тем самым создаются условия для образования мелкозернистой структуры. Рассеивающая способность электролита вследствие высокой поляризуемости и снижения выхода по току при повышении плотности тока весьма хорошая. [44]
Цементация германия происходит после выделения меди и до выделения кадмия. Широкому применению этого метода мешают, в частности, большие потери германия в виде летучих гидридов, улавливание которых затруднительно. По данным [19], высокая кислотность раствора, избыток цинковой пыли при цементации, а также присутствие меди и мышьяка в растворе повышают улетучивание германия. [45]
Страницы: 1 2 3 4