Выделение - кадмий
Cтраница 4
Во многих случаях для отделения кадмия его осаждают в виде сульфида. Большие концентрации галоидных солей в кислой среде мешают выделению кадмия в виде сульфида. Сероводород при низкой кислотности, повидимому, отделяет малые количества кадмия от больших количеств никеля и кобальта. [46]
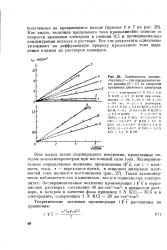 |
Зависимость плотио-ститока ( 7 - - о и предельного тока кадмия ( 6 - 1 ] от скорости вращения дискового электрода. [47] |
Как видно, величина предельного тока прямолинейно зависит от скорости вращения электрода в степени 0 5 и пропорциональна концентрации металла в растворе. Все эти результаты однозначно указывают на диффузионную природу предельного тока выделения кадмия из растворов цианидов. [48]
Соответственно нормальному потенциалу в ряду напряжений располагается между железом и цинком. Следовательно, галлий из его кислых растворов может цементироваться такими металлами, как алюминий и цинк, причем выделяется он после выделения кадмия. [49]
Такое влияние плотности тока на состав катодного осадка должно быть объяснено следующим. Однако выделение кадмия на катоде протекает с значительно меньшей поляризацией, чем выделение олова. Поэтому увеличение плотности тока сопровождается уменьшением его доли, приходящейся на выделение олова, и содержание его в осадке падает. [50]
Для удаления воды электроды погружают в ацетон и катод затем высушивают на воздухе или на несколько минут помещают его в сушильный шкаф при 100 С. Заключительное взвешивание позволяет определить количество меди по увеличению массы электрода. Для выделения кадмия анод и покрытый медью катод ( гладкая платина легко легируется некоторыми металлами, например Cd, Hg, Sn, Zn, Bi, и очень трудно очищается после этого) снова погружают в электролизуемый раствор. Источниками напряжения служат два последовательно включенных аккумулятора; силу тока 0 5 А устанавливают с помощью регулируемого сопротивления. Каково должно быть напряжение на клеммах для количественного выделения Cd. [51]
Для определения кадмия, присутствующего в растворе наряду с таллием, используют ртутный катод и платиновый анод. Потенциал ртутного катода должен обеспечивать разряд только ионов кадмия. Окончание выделения кадмия определяют по падению силы тока до постоянной величины. Количество протекшего электричества находят по кулонометру, включенному последовательно с электролизером, а затем, зная электрохимический эквивалент кадмия, вычисляют его содержание в растворе. Если в том же растворе необходимо определить также и таллий, то, сместив потенциал ртутного катода до требуемой величины, проводят анализ, как для кадмия. [52]
Страницы: 1 2 3 4