Выделение - молекулярный кислород
Cтраница 1
Выделение молекулярного кислорода на платине наступает при потенциале 1 85 в. Таким образом, из измерений, проведенных в переменном токе, следует, что процессу выделения кислорода на платине предшествует образование на поверхности электрода высшего кислородного соединения. [1]
Обратите внимание на выделение молекулярного кислорода во всех тех реакциях, где перекись водорода проявляет восстановительные свойства. [2]
Эубактерий, фотосинтез которых сопровождается выделением молекулярного кислорода ( цианобактерии и прохлорофиты), содержат хлорофиллы, характерные для фотосинтезирующих эука-риотных организмов. Присутствие этих пигментов обеспечивает поглощение света до 750 нм. [3]
При каталитическом воздействии перборат натрия может распадаться с выделением молекулярного кислорода, теряя тем самым свое отбеливающее свойство. Каталитический распад пербората натрия зависит от температуры; при температуре 40 С практически не наблюдается распад пербората натрия, а при температуре 95 С за 1 ч теряется половина активного кислорода. [4]
Возрастание тока при Ет 1 45 В отвечает процессу выделения молекулярного кислорода. При изменении потенциала в катодном направлении наблюдаются четкий максимум восстановления адсорбированного кислорода, слабо выраженная двойнослойная область и максимумы посадки адсорбированного водорода. Максимумы ионизации - посадки водорода - при менее анодном потенциале, называют максимумами слабо связанного водорода, а более анодные максимумы - максимумами прочно связанного водорода. [5]
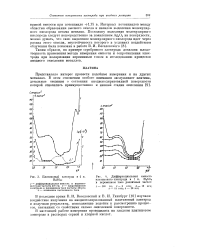 |
Платиновый электрод в 1 н. H2S04.| Дифференциальная емкость платинового электрода в н. HaSCU в переменном токе различных частот. [6] |
Интервал потенциалов между областью образования высшего окисла и началом выделения молекулярного кислорода весьма невелик. [7]
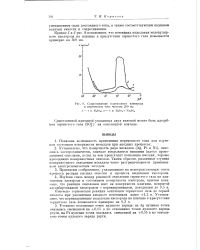 |
Сопротивление платинового электрода в переменном токе частоты 200 гц. [8] |
Кривые 1 и 2 рис. 8 показывают, что потенциал выделения молекулярного кислорода на платине в присутствии сернистого газа Повышается примерно на 300 мв. [9]
При повышении температуры или уменьшении парциального давления кислорода диоксигенилы разрушаются с выделением молекулярного кислорода. [10]
Поэтому при окислительно-восстановительных реакциях окисление озоном происходит за счет третьего атома кислорода с выделением молекулярного кислорода. [11]
А из этого следует, что и в этом случае должно иметь место разложение Н202 с выделением молекулярного кислорода, как и в случае каталазы. Но, как показали впервые Бах и Шода, пероксидаза, в отличие от каталазы, не выделяет из Н202 ни следа молекулярного кислорода - - наблюдение, подтвержденное самим Вильштеттером на его чистейших препаратах пероксидазы. [12]
Другие авторы [2] показали, что при некоторых потенциалах, лежащих внутри интервала потенциалов, в котором эти авторы измеряли скорость выделения молекулярного кислорода, на исследованных металлах образуются поверхностные окислы; на основании этого они утверждают, что выделение кислорода происходит путем образования и распада высших окислов. [13]
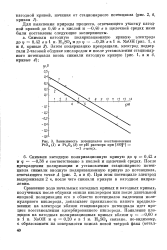 |
Зависимость потенциалов восстановления. [14] |
Сравнение хода начальных катодных кривых и катодных кривых, полученных после обдувки окисла кислородом или после длительной анодной поляризации его в области потенциалов выделения молекулярного кислорода, доказывает правильность нашего предположения: на электроде вблизи стационарного потенциала идет процесс восстановления адсорбированного кислорода. [15]
Страницы: 1 2 3 4