Выделение - полоний
Cтраница 1
Выделение полония из растворов радия проводится, как и из растворов активного налета радона, электрохимическим методом. [1]
Выделение полония на серебре происходит медленно. Выделение на металлическом никеле, благодаря большой разнице в значениях потенциалов, происходит более энергично, но полоний будет загрязнен RaE. Разделение полония и RaE может быть выполнено возгонкой полония на другую охлаждаемую пластинку. [2]
Выделение полония на серебре или никеле производится из кислых растворов, в которых не происходит гидролиза. Извлечению мешает присутствие большого количества посторонних солей, в особенности трехвалентного железа и других металлов переменной валентности. [3]
Выделение полония на серебре из раствора НС1 наиболее значительно и соответствует большому количеству монослоев. Для осаждения полония из солянокислого раствора изучена зависимость выделяющегося количества полония от количества его в растворе, а также от температуры. Эрбахер предположил, что скорость выделения путем образования смешанных кристаллов зависит от двух факторов. С одной стороны, она обратно пропорциональна скорости образования Ag202 ( чем больше эта скорость, тем меньше полония успевает войти в кристаллическую решетку перекиси), которая, очевидно, зависит от количества образовавшегося озона, или, другими словами, от содержания полония в растворе. С другой стороны, скорость осаждения полония прямо пропорциональна скорости диффузии ионов полония к электроду, которая увеличивается с повышением температуры раствора. Действительно, в результате экспериментов было доказано, что относительная скорость осаждения полония на серебре уменьшается с увеличением содержания полония в растворе и увеличивается при повышении температуры. [4]
Выделение полония может быть осуществлено и на платине в присутствии восстанавливающих агентов ( хинона, гидрохинона) или на платине, насыщенной водородом, из разбавленных растворов соляной кислоты. [5]
Для выделения полония из урановых руд последнюю сплавляют с содой, плав выщелачивают водой, при этом полоний переходит в раствор вместе с рядом других элементов в виде солей соответствующих кислот. Раствор подкисляют НС1 и из него осаждают сульфиды металлов с помощью сероводорода, при этом в осадок выделяются наряду с полонием висмут, ртуть, сурьма, олово, мышьяк, таллий, свинец. Осадок промывают сернистым или многосернистым аммонием для удаления сульфидов олова, мышьяка и сурьмы, затем растворяют в азотной кислоте и нейтрализуют. При последующем разбавлении водой висмут образует малорастворимую основную соль Bi ( OH) ( N0) 3) 2, с которой соосаждается полоний. В качестве примесей при этом присутствуют таллий и свинец. Осадок растворяют в азотной кислоте и полоний из раствора осаждают на серебре. Дальнейшее выделение проводят по вышеописанному способу. [6]
Для выделения полония из урановой руды его переводят в раствор в виде РоС и восстанавливают сероводородом или активными металлами на платиновых или цинковых пластинках. Полоний - серебристо-белый с желтоватым оттенком мягкий металл с температурой плавления 254 С. Низкотемпературная - модификация - простая кубическая решетка - при 36 С переходит в ромбоэдрическую / - модификацию. При горении на воздухе образует оксид РоО2 - самый стабильный из всех оксидов полония. Производные Ро ( 6) характеризуются кислотной функцией. [7]
Для выделения полония из урановой руды его переводят в раствор в виде РоС12 и восстанавливают сероводородом или активным металлами на платиновых или цинковых пластинах. Компактный полоний - серебристо-белый с желтоватым оттенком мягкий металл с температурой плавления 254 С. Низкотемпературная а-модификация - простая кубическая решетка - при 36 С переходит в ромбоэдрическую 3-модификацию. [8]
Для выделения полония из урановой руды его переводят в раствор в виде РоС и восстанавливают сероводородом или активными металлами на платиновых или цинковых пластинках. Полоний - серебристо-белый с желтоватым оттенком мягкий металл с температурой плавления 254 С. Низкотемпературная ( модификация - простая кубическая решетка - при 36 С переходит в ромбоэдрическую / 3-модификацию. При горении на воздухе образует оксид РоО2 - самый стабильный из всех оксидов полония. При анодном окислении полония получается РоОз - Производные Ро ( 6) характеризуются кислотной функцией. [9]
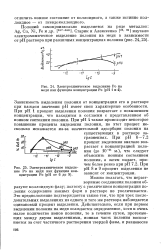 |
Электрохимическое выделение Ро на меди как функция концентрации Ро ( рН 1 и 4.| Электрохимическое выделение Ро на меди как функция концентрации Ро ( рН от 6 до 9. [10] |
Зависимость выделения полония от концентрации его в растворе при каждом значении рН имеет свои характерные особенности. При рН 1 процент выделения полония возрастает с повышением концентрации, что находится в согласии с представлением об ионном состоянии полония. [11]
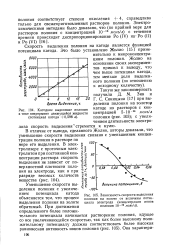 |
Катодное выделение полония.| Зависимость скорости выделения полония на золоте от величины потенциала электрода ( концентрация ионов полония 10 - 10 моль. А. [12] |
Скорость выделения полония на катоде является функцией потенциала катода. Это было установлено Жолио [15] применительно к микроконцентрациям полония. [13]
В процессе выделения полония из урановой смолки ( см. разд. [14]
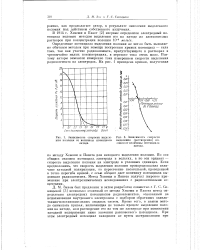 |
Зависимость скорости выделе - [ IMAGE ] Зависимость скорости. [15] |
Страницы: 1 2 3 4