Выделение - галлий
Cтраница 2
Присутствие в растворе мышьяка и галлия не препятствует определению; для предотвращения гидролитического выделения галлия вводится лимонная кислота. [16]
Электролизом водных растворов можно отделить галлий от многих металлов Поддерживая катодный потенциал меньшим потенциала выделения галлия, можно выделить из раствора более электроположительные элементы, оставляя галлий и другие электроотрицательные элементы в растворе. Во всех случаях получается плотный спектральночистый мелкокристаллические осадок меди. [17]
Эта температура соответствует температуре, при которой экспериментально было зафиксировано полное диспропорционирование GaCl с выделением галлия на стенках конденсатора. Из рис. 4 видно, что при уменьшении температуры реакции фронт диспропорционирования перемещается в зоне реакции, приближаясь при 673 К к реакционной зоне. Этот факт свидетельствует о том, что уже при этой температуре монохлорид галлия не транспортируется из реакционной зоны. [19]
Присутствие многоатомных спиртов жирного ряда ( маннит и глицерин) не оказывает влияния на полноту выделения галлия. [20]
К наименее растворимым соединениям галлия относится его ферроцианид, образованием которого воспользовался еще Лекок де Буабодран при выделении галлия из кислых растворов. Состав ферроцианида галлия установлен И. В. Тананаевым и Н. В. Баусо-вой, разработавшими также амперометрический метод определения галлия по току окисления ферроцианида на платиновом электроде. Ре ( СЫ) б ] з - Растворимость ферроцианида галлия очень мала - можно определять до 10 мкг галлия в титруемом объеме. Алюминий, который почти всегда сопутствует галлию в растворах, не мешает титрованию, хотя при относительно больших количествах алюминия величина тока окисления ферроцианида заметно понижается, вследствие чего определение конечной точки становится менее отчетливым. Влияние алюминия было замечено и при других титрованиях и может быть устранено титрованием с таким электродом сравнения, потенциал которого лишь не намного отличался бы от потенциала окисления ферроцианида, например с перманганатным электродом ( см. гл. [21]
Экстракция галлийхлористоводородной кислоты из разбавленной ( 1: 1) соляной кислоты этиловым или изопропиловым эфиром имеет большое практическое значение для выделения галлия. Коэффициент распределения галлия для системы этиловый эфир - 6 М соляная кислота равен - 17 ( стр. Применяя извлечение эфиром, галлий отделяют от алюминия а и цинка ( хотя и сообщают, что экстрагируются следы цинка), а также от многих других металлов. К металлам, хлориды которых извлекаются эфиром, относятся железо ( Ш), золото, таллий ( Ш), германий, молибден, рений, мышьяк, сурьма и олово ( ср. Медь ( П) экстрагируется в небольшом количестве. [22]
Так как при электролизе с ртутным катодом натрий выделяется одновременно с галлием и цементация на образовавшейся натриевой амальгаме является одним из путей выделения галлия из раствора, было предложено разделить эти процессы: сначала получать натриевую амальгаму, затем цементировать на ней галлий. [23]
Хиршем и С. С. Лиангом ( патент США 4 071422, 31 января 1978 г., фирма чКоминко Лтд, Канада), предназначен для выделения галлия и других ценных компонентов из дымной пыли фосфорного производства путем обработки ее серной кислотой с образованием раствора и твердого остатка. Цинк осаждается из раствора в виде аммонийно-1. [24]
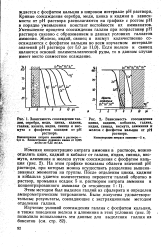
Изучение условий соосаждения галлия с фосфатом кальция, а также поведения железа и алюминия в этих условиях ( рис. 3) позволило использовать эти данные для выделения галлия из бокситов ( см. стр. [26]
Нормальный ( стандартный) электродный потенциал галлия, измеренный по отношению к 1 N Ga2 ( S04) 3, равен-0 58 в [1259] ( по другим данным - 0 52 в [725]), вследствие чего выделение галлия из кислого раствора затруднительно, однако из щелочного раствора возможно. [27]
Для определения в виде Ga203 выделяют из раствора гидроокись галлия, либо основные соли, адсорбционные соединения гидроокиси с коллоидными кислотами или солями или внутри-комплексные соединения с органическими кислотами. Выделение галлия в виде гидроокиси Ga ( OH) 3 разбавленным раствором аммиака представляет некоторые трудности, поэтому иногда предпочитают гидролитические методы выделения либо осаждение органическими реагентами, а также образование труднорастворимых адсорбционных соединений. [28]
Поэтому облучение пробы проводится в кварцевой ампуле с притертой пробкой, что облегчает операцию извлечения пробы после облучения. Для выделения галлия используется простая экстракционная методика в экстракторе с дистанционным управлением. После сброса высокой активности основы органическая фаза с извлеченным галлием передается в соседнюю лабораторию, где в более удобных условиях проводится дополнительная радиохимическая очистка. [29]
Галлий из слабокислых растворов в условиях осаждения, описанных нами для других металлов, в отсутствие хлористого аммония количественно не осаждается. Присутствие NtUCI повышает степень выделения галлия, но все же не приводит к количественному осаждению. Исследование этого явления показало следующее. [30]
Страницы: 1 2 3 4