Анодное выделение - кислород
Cтраница 3
В дальнейшем нами были проведены опыты по анодному выделению кислорода непосредственно в молекулярной форме. При этом поверхность никеля покрыта слоем гидрата закиси Ni ( OH) 2, а на поверхности серебра фазовые окислы вообще отсутствуют. [31]
К этой же группе процессов следует отнести и анодное выделение кислорода, если только его скорость определяется стадиями образования или распада высших окислов электродного металла. [32]
К этой же группе процессов следует отнести и анодное выделение кислорода, если его скорость определяется, например, стадиями образования ( или распада) высших окислов электродного металла. [33]
Еще в 1940 г. мною было показано, что в процессе анодного выделения кислорода происходит изменение состояния поверхности платинового анода, причем кинетика выделения кислорода зависит от степени окисленности электрода. Если поляризацию платинового электрода, катодно восстановленного, начать малыми токами и идти в сторону больших токов ( в 1 Л 112804), а значения потенциала анода фиксировать через 15 мин. При этом прямой и обратный ход кривых практически совпадают между собой. [34]
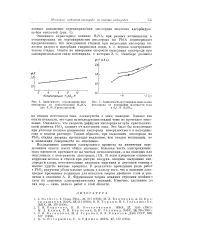 |
Зависимость перенапряжения.| Зависимостыютенциала выделения. [35] |
К этим процессам относятся коррозия железа и сталей при доступе воздуха, анодное выделение кислорода и хлора, восстановление двуокиси марганца и двуокиси свинца и многие другие важные процессы. В результате проведения ряда работ с РЬ02 получены убедительные доводы в пользу того, что к окисным электродам применима созданная для металлов теория двойного слоя и развитая в основном А. Н. Фрумкиным теория влияния строения двойного слоя на кинетику электрохимических реакций. Конечно, сделанное до сих пор - лишь начало работ в этой области. [36]
Существует мнение, впервые высказанное Ферстером ( 1909), согласно которому анодное выделение кислорода во всех случаях совершается только через образование промежуточных неустойчивых окислов. Переход последних в устойчивые окислы ( или в состояние исходного металла с одновременной потерей кислорода, выделяющегося в газообразном виде) определяет кинетику всей электродной реакции. Таким образом, появление кислородного перенапряжения вызывается многими причинами и может быть связано с замедленным протеканием одной из следующих стадий: разряда ионов гидроксила или молекул воды, рекомбинации атомов кислорода, электрохимической десорбции гидроксильных радикалов ОН, образования и распада неустойчивых промежуточных окислов электродного металла. [37]
Значительное влияние на скорость коррозии решеток положительного электрода свинцового аккумулятора оказывает процесс анодного выделения кислорода. [38]
Если производится восстановление с одновременным выделением на катоде водорода или окисление с анодным выделением кислорода, то контроль потенциала становится излишним и достаточно работать при постоянной плотности тока. Однако, так как растворимость большинства органических соединений в воде мала, то зачастую приходится использовать раствор соответствующего электролита ( минеральной кислоты, неорганического или органического основания, соли-уксуснокислого калия, хлористого лития и др.) в смешанном ( водно-неводном) растворителе, например вода-спирт или вода-уксусная кислота. Нередко в более сложных системах применяется спирт, уксусная кислота или смесь дихлорэтана и уксусной кислоты, с соответствующим электролитом. Какова бы ни была электропроводность таких систем, относительный потенциал рабочего электрода в них значительно выше того, какой требуется для выделения газов из водных растворов. [39]
Суммарные уравнения ( I) и ( 1а) справедливы также для реакции анодного выделения кислорода, которая является обратной реакции электровосстановления кислорода. [40]
Принимая во внимание возможность того, что нормальный разряд гидроксильного иона, приводящий к анодному выделению кислорода, является результатом перехода протона из молекулы воды, адсорбированной на поверхности электрода, можно полагать, что молекулы воды в значительной степени вытесняются ацетатными ионами. Разряд гидроксильных ионов с образованием кислорода затрудняется и не происходит до тех пор, пока потенциал не достигнет значения, достаточного для разряда ацетатных ионов и последние будут удалены с поверхности анода. Если введением в среду нейтральных солей предотвратить накопление у электрода ацетатных ионов, то их адсорбция будет относительно мала, и разряд гидроксильных ионов будет происходить при нормальном потенциале. Присутствие катализаторов разложения перекиси водорода, вероятно, благоприятствует разряду гидроксильных ионов, так как облегчает образование кислорода. Таким образом, могут быть объяснены наблюдаемые при этом низкие потенциалы. [41]
В качестве материалов для инертных анодов употребляется платина и нержавеющая сталь, на которых происходит анодное выделение кислорода. [42]
Электрохимический процесс окисления, как правило, является не единственным при электролизе и всегда сопровождается анодным выделением кислорода. Следовательно, расход электрической энергии распределяется между этими двумя процессами. Преобладание одного из них зависит от величин потенциала окисления вещества и потенциала выделения кислорода, причем преобладать будет тот процесс, который идет более легко, при меньшем потенциале. [43]
Электрохимический процесс окисления, как правило, является не единственным при электролизе, но всегда сопровождается анодным выделением кислорода, и, таким образом, энергия распределяется между двумя процессами. [44]
При электролизе графит изнашивается не в результате основного электрохимического процесса - процесса окисления хлор-иона, а вследствие анодного выделения кислорода. Кислород в момент выделения окисляет графит до COs. Износ анодов возникает не только как следствие выгорания углерода, но и из-за осыпания графитовой массы после того, как ослаблена в результате выгорания механическая связь поверхностного слоя графита с телом анодов. Различают поэтому химический и механический износ анодов. Часть графита анодов уходит также в огарки. [45]
Страницы: 1 2 3 4