Акваион
Cтраница 2
Повышение эффективности может явиться следствием высвобождения парамагнитного акваиона железа ( III) из комплекса и образования гидроксилсодержащих комплексов. В выбранных условиях эксперимента ( рН близко к нейтральной, высокая концентрация винной кислоты) образование гидроксилсодержащих комплексов ионов железа при добавлении ионов галлия исключено. [16]
Видно, что внутренняя координационная сфера этих акваионов длительное время существует в виде стабильного образования. [17]
 |
Пространственная конфигурация комплексов. [18] |
Действительно, реакция вытеснения воды аммиаком из внутренней сферы акваиона протекает в водном растворе довольно легко. [19]
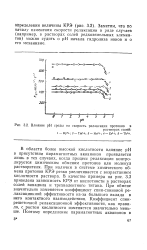 |
Влияние рН среды на скорость релаксации протонов в. [20] |
В области более высокой кислотности влияние рН в присутствии парамагнитных акваионов проявляется лишь в тех случаях, когда процесс релаксации контролируется химическим обменом протонов или молекул растворителя. При наличии в системе химического обмена протонов КРЭ резко увеличивается с возрастанием кислотности раствора. В качестве примера на рис. 3.3 приведена зависимость КРЭ от кислотности в растворах солей ванадила и трехвалентного титана. При обмене значительно изменяется коэффициент спин-спиновой релаксационной эффективности из-за большого вклада в него контактного взаимодействия. Коэффициент спин-решеточной релаксационной эффективности, как правило, с ростом кислотности изменяется значительно меньше. [21]
Известно, что в водных растворах ионы металлов находятся в виде акваионов ( аквакомплексов) типа М ( Н20), где N - координационное число иона металла, п - его заряд. Обычно число координированных ионом металла молекул воды равно его координационному числу, причем по своему происхождению связь металл-атом кислорода в молекуле воды является донорно-акцепторной. [22]
Если, например, к раствору сульфата меди, обладающему синей окраской акваионов Си2, добавлять раствор, содержащий ионы CN -, то вначале выпадает желтый осадок Cun ( CN) 2, который при добавлении избытка ионов CN - растворяется с образованием бесцветного раствора. Из этого наблюдения можно сделать вывод, что образуются цианокомплексы меди. [23]
Высокое перенапряжение металлов железной группы объясняется тем, что электронная структура их разряжающихся акваионов значительно отличается от структуры соответствующего металла. Напротив, электронные структуры нормальных металлов в кристалле и в водных комплексах близки, и поэтому они обладают низким перенапряжением. [24]
Присутствие в растворе повышенных количеств диамагнитных солей не влияет на релаксационную эффективность парамагнитных акваионов или это влияние может быть учтено. Данное обстоятельство, а также сходство по ряду химических свойств парамагнитных и диамагнитных ионов позволяет использовать влияние последних на равновесие системы парамагнитной ион - лиганд для изучения состава и устойчивости диамагнитных комплексов. [25]
Таким следствием является, например, повышенная скорость обмена двух аксиальных молекул воды акваиона [9], а это, в свою очередь, согласно [37] может вызвать некоторое дополнительное увеличение объема по сравнению с другими системами, обладающими таким же механизмом обмена, но меньшей его скоростью. Исключение, возможно, составляет только никель. [26]
Здесь же, рассматривая чувствительность метода, следует отметить, что при образовании парамагнитным акваионом комплекса величина его / Сэ1 уменьшится на один-два порядка. [27]
Джисл) м и ( восст) м - константы диффузии окисленной и восстановленной форм простого акваиона. [28]
Возможность оценки минимальной концентрации по приведенному соотношению была проверена на примере определения концентраций в растворах акваионов марганца, меди, никеля, кобальта. [29]
Если молекула воды является слишком сильным конкурентом для лиганда, то он с трудом вытесняет ее из акваионов. Проведение синтеза в растворителе, обладающем меньшим сродством к иону металла, позволяет получить комплексы с вводимым лиган-дом. Из водных растворов выделить эти соединения не удается. При взаимодействии ( Me4N) iNO3 с Со ( МО3) 2 - 2Н2О в соотношении 2: 1 в нитрометане получено соединение ( Me4N) 2 [ Co ( NO3) 4 ] фиолетового цвета. Из водных растворов нитратные комплексы Со2, тем более с КЧ 4, не выделены. [30]
Страницы: 1 2 3 4