Акваион
Cтраница 4
Некоторые из выведенных уравнений [ например, ( VI, 24), ( VI, 42) - ( VI, 44), ( VI, 60), ( VI, 61) ] справедливы только в том случае, если диффузионные константы комплексного иона и простого акваиона металла или окисленной и восстановленной форм комплекса различаются незначительно. В соответствующих выражениях отношение этих констант приближенно принято равным единице. Если константы сильно различаются, то их отношение должно быть учтено в уравнениях. [46]
С акваионом Fe2 - aq; желтая кровяная соль дает серый осадок, синеющий во времени из-за окислительного взаимодействия с кисло-родом воздуха. С акваионом Fe - aq красная кровяная соль образует буро-зеленый раствор. Гексацианиды железа предложено использовать для разделения смесей РЗЭ методом фракционного осаждения. [47]
Объектами спектрофотометрического изучения могут быть растворы различных соединений, как органических, так и неорганических. Однако величины поглощения неорганических акваионов обычно очень малы, поэтому в практике спектрофотометрии используют различные химические реакции образования соединений, растворы которых обладают значительно большими поглощающими свойствами. [48]
Кинетическая инертность или лабильность акваионов обусловливает выбор способа титрования - прямое или обратное. Образование лабильных комплексов ионов с металлоиндикатором обеспечивает быстрое изменение окраски раствора в конечной точке титрования. Соединение кобальта с ПАН-2 кинетически инертно, поэтому ПАН-2 не используют в качестве индикатора при определении кобальта прямым методом. На скорость изменения окраски раствора в конечной точке титрования влияют природа и концентрация буферного раствора. [49]
Поэтому пропускание раствора, содержащего комплексы состава [ МП1А ] смеси РЗЭ через колонку с катионообменной смолой приводит к тому, что ионы М3 различных РЗЭ в неодинаковой степени задерживаются в смоле. Ионы М3 ( в форме акваионов, например [ Мш ( Н2Э) д ] 3), легких РЗЭ, комплексы [ МША ] - которых относительно сильно диссоциируют, содержатся в растворе в большей концентрации, чем ионы М3 тяжелых РЗЭ. Понятно, что в большей мере поглощаются ионообменной смолой и медленнее проходят через слой катио-нита ионы М3 именно легких РЗЭ. [50]
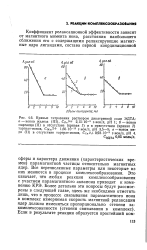
При избытке лйганда X на полярограмме образуется только одна ступень. Она может находиться положительнее или отрицательнее ступени акваиона. При таких условиях могут быть сделаны только качественные выводы о процессе комплексообразования. [51]
Природа лиганда слабо отражается на величине kc, но металл влияет на эту константу. Значения kc для щелочных металлов указывают на лабильность их акваионов. [52]
Все перечисленные параметры или некоторые из них меняются в процессе комплексообразования. Это означает, что любая реакция комплексообразования с участием парамагнитного акваиона приводит к изменению КРЭ. [54]
Это делает возможным их выделение из водных растворов в отличие от таких металлов, как титан, цирконий и др., ионы которых в растворе присутствуют в виде внутриорбитальных комплексов. Высокое перенапряжение металлов группы железа объясняется тем, что электронная структура их разряжающихся акваионов значительно отличается от структуры соответствующего металла. Электронные структуры нормальных металлов в кристалле и в водных комплексах близки, и поэтому они обладают низким перенапряжением. [55]
Это делает возможным их выделение из водных растворов, в отличие от таких металлов, как титан, цирконий и др., ионы которых в растворе присутствуют в виде внутриорбиталъных комплексов. Высокое перенапряжение металлов железной группы объясняется тем, что электронная структура их разряжающихся акваионов значительно отличается от структуры соответствующего металла. Напротив, электронные структуры нормальных металлов в кристалле и в водных комплексах близки, и поэтому они обладают низким перенапряжением. [56]
Страницы: 1 2 3 4