Дифторид - ксенон
Cтраница 1
Дифторид ксенона XeF2 впервые был получен облучением смеси ксенона и фтора ультрафиолетовыми лучами. [1]
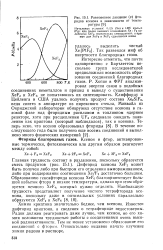 |
Равновесное давление ( р фторидов ксенона в зависимости от температуры. [2] |
Дифторид ксенона XeF2 может быть получен либо при быстром его отделении вымораживанием, либо при поддержании соотношения Xe / F2 достаточно большим. Образованию гексафторида ксенона XeF6 благоприятствует большой избыток фтора и низкие температуры, однако при этом образуется немного XeF4, который нужно отделять. [3]
Молекула дифторида ксенона имеет линейную структуру. [4]
Окислительно-восстановительные потенциалы дифторида ксенона / / Журн. [5]
При действии дифторида ксенона на пиперидиноксилы образуются фториды оксопиперидиния в смеси с нитрозосоединениями. [6]
Изучение реакционной способности промежуточной частицы гидролиза дифторида ксенона методом конкурентных реакций / / Журн. [7]
Проведенные исследования показали, что при введении дифторида ксенона и фторидов редкоземельных элементов, а также фторидов цинка и железа температура начала разложения обоих сополимеров сдвигается в область более высоких температур. Одновременно увеличивается продолжительность эксплуатации по сравнению с исходными сополимерами. При введении оксалатов металлов заметно повышается температура начала разложения только сополимера винилиденфторида с трифторхлорэтиленом на деструкцию сополимера винилиденфторида с тетра-фторэтиленом они влияния не оказывают. [8]
 |
Свойства фторидов ксенона. [9] |
В и говорит о том, что по окислительной способности дифторид ксенона превосходит озон. [10]
Советские химики В. М. Хуторецкий и В. А. Шпанский показали, что для синтеза дифторида ксенона совсем не обязательны жесткие условия. [11]
При взаимодействии ксенона с фтором в зависимости от условий опыта получается либо дифторид ксенона Хер2, либо теграфторид XeF4, либо гекса-фторид XeFg. [12]
В декабре 1962 г. было сообщено, что в результате фотохимической реакции получен дифторид ксенона XeFg. Первой стадией в этой реакции, вероятно, являлась диссоциация молекулы фтора на два атома фтора в результате поглощения фотона, имеющего энергию, достаточную для того, чтобы вызвать диссоциацию. Чему равна максимальная длина волны света, который может вызвать эту фотохимическую реакцию, если такой свет будет поглощен. [13]
Моно - и дифторпроизводные ароматических соединений в ряде случаев могут быть легко получены при действий дифторида ксенона на ароматические углеводороды. [14]
 |
Галогенат-ионы в твердых солях. [15] |
Страницы: 1 2