Выпаривание
Cтраница 4
Выпаривание широко применяется для повышения концентрации разбавленных растворов или выделения из них растворенного вещества путем кристаллизации. [46]
Выпаривание ведут как под атмосферным, так и под пониженным или повышенным давлением. [47]
Выпаривание под давлением связано с повышением температуры кипения раствора, поэтому применение данного способа ограничено свойствами раствора и температурой нагревающего агента. [48]
Выпаривание может быть простым, а также одно - и многступен-чатым под вакуумом. Простое выпаривание производят в открытых резервуарах, в которых сточная вода с помощью пара низкого давления нагревается до 100 С, что вызывает большой расход теплоты. При выпаривании под вакуумом можно значительно снизить температуру кипения раствора и, следовательно, использовать в качестве источника теплоты отработанный пар, однако вакуумные выпарные установки более сложны в аппаратурном оформлении, а также при эксплуатации. [49]
Выпаривание широко применяют для концентрирования водных растворов щелочей ( едкий натр, едкое кали), солей ( iNaCl, Na2S ( 4, NH4N03 и др.) и некоторых высококипящих жидкостей. Выпаривание применяют также для получения растворителя в чистом виде, например для опреснения морской воды, однако этот способ довольно дорог и в настоящее время заменяется другими, более дешевыми. [50]
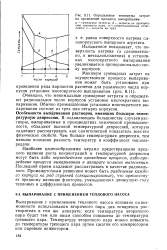 |
Определение минимума затрат на проведение процесса выпаривания. [51] |
Выпаривание с применением теплового насоса основано на возможности использования вторичного пара для испарения растворителя в том же аппарате; если температура вторичного пара будет тем или иным способом повышена до температуры греющего пара. [52]
Выпаривание ведут как под атмосферным, так и под повышенным или пониженным давлением. В первом случае образующийся вторичный ( соковый) пар выводится в атмосферу. [53]
Выпаривание осуществляется в аппарате с погружной горелкой теплопроизводительно-стью 400000 ккол / ч ( фиг. [54]
Выпаривание представляет собой самый простой способ концентрирования. Если нагревать, например, 100 мл или больший объем анализируемого раствора, то по мере испарения растворителя концентрация раствора повышается; при доведении объема жидкости до 0 1 мл концентрация находящегося в ней вещества повышается в 103 раз. Такой способ концентрирования применяют при определении примеси тяжелых металлов в питьевых водах. Несмотря на простоту, этот способ находит ограниченное применение. Исследуемый раствор наряду с малыми концентрациями определяемых веществ обычно содержит довольно большие количества других соединений. Поэтому выпаривание до очень малых объемов иногда вообще невозможно, из-за выделения растворенных веществ. Во всяком случае при выпаривании вместе с повышением концентрации определяемых веществ повышается и концентрация всех других веществ, находящихся в анализируемой жидкости, отделение примеси от сопутствующих веществ не достигается. [55]
Выпаривание проводят в вытяжном шкафу. К остатку после выпаривания добавляют 1 мл концентрированной соляной кислоты и снова выпаривают досуха. Полученный остаток растворяют в дистиллированной воде, подогревая смесь, если понадобится. Затем фильтруют через стеклянную фильтрующую пластинку и анализируют фильтрат описанным ниже методом. [56]
Страницы: 1 2 3 4