Высота - энергетический барьер
Cтраница 3
В химической кинетике свободная энергия активации рассматривается как высота энергетического барьера, который необходимо преодолеть реагирующим веществам, чтобы произошла реакция. В случае электрохимических реакций AG представляет собой высоту энергетического барьера, который необходимо преодолеть электрону при движении между электроактивным веществом и электродом. [31]
Были проведены расчеты энергии в узле решетки, высоты энергетического барьера и энергии испарения с использованием закона взаимодействия 1 / г6 и с учетом взаимодействия с ближайшими соседями до четвертого порядка. Расчеты показали, что молекула совершает в среднем 105 скачков по поверхности, прежде чем снова испарится. Если это верно, то скорость роста кристаллов по механизму повторимого шага должна чрезвычайно сильно возрасти, поскольку адсорбированные молекулы с большой площади будут питать положение повторимого шага, а также способствовать образованию двумерного зародыша. [32]
Особенность электрохимического процесса состоит в том, что высоту энергетического барьера можно изменять, меняя потенциал электрода. [33]
Следовательно, величины Q и Q определяют собой высоту энергетического барьера реакции, ее энергию активации, в зависимости от того, какая из них будет иметь более низкое или более отрицательное значение. [34]
 |
Поверхность потенциальной энергии для взаимодействия трех атомов. [35] |
Однако одному из этих путей отвечает наименьшая из возможных высота энергетического барьера, требующая, следовательно, наименьших энергетических затрат. Данный путь является, естественно, наиболее выгодным путем, он и есть координата реакции, а точка, отвечающая вершине барьера - активированный комплекс. [36]
Три фактора определяют скорость элементарной реакции: а) высота энергетического барьера, б) вероятность или энтропия активированного комплекса ив) динамические эффекты. [37]
Для того чтобы определить стабильные конформаций, а также высоты энергетических барьеров вращения вокруг простых связей, ряд простых производных и аналогов этана был исследован термохимическим, спектральным и другими физическими методами. Если производное этана имеет шесть заместителей, связанных простыми связями, оно всегда существует предпочтительно в заторможенной конформаций. Однако если число заместителей уменьшить до пяти ( один заместитель связан двойной связью), то одна простая связь заслоняется двойной связью. Эти стабильные конформаций показаны ниже в виде проекций Ньюмена. [38]
Здесь U представляет собой энергию активации перемещения и равна высоте энергетического барьера между двумя последовательными положениями вакантного узла. [39]
Этот процесс, идущий с определенной скоростью, зависящей от высоты энергетического барьера, разделяющего оба равновесных положения водородного атома, также должен был бы вести к частичному превращению ( а) в ( Ь), которое, как мы сейчас увидим, могло бы быть обнаружено с помощью меченых атомов. [40]
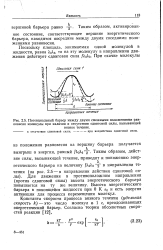 |
Потенциальный барьер между двумя смежными положениями равновесия молекулы при наличии и отсутствии сдвиговой силы, вызывающей. [41] |
Для движения в противоположном направлении ( против сдвиговой силы) высота энергетического барьера повышается на ту же величину. Высота энергетического барьера в покоящейся жидкости при О К БО и есть энергия активации для процесса перемещения молекул. [42]
 |
К понятию энергии активации. [43] |
Следовательно, теория элементарного химического акта должна давать возможность расчета высоты энергетического барьера и вероятности образования переходного состояния исходя из строения и свойств реагирующих молекул. Одним из первых направлений в развитии теории элементарных реакций является теория активных столкновений. [44]
А - константа; те - масса электрона; W - высота энергетического барьера, под которым туннелируют электроны; h - постоянная Планка. [45]
Страницы: 1 2 3 4