Выход - амид
Cтраница 1
Выход амида а - ( 1М - метил - ] - фениламино) - р-бензошшропионовой кислоты 0 8 г ( 75 4 % от теорет. [1]
Выход амидов XXVIII и XXIX составляет 77 и 82 % соответственно. В молекуле этаноламина имеются два реакционных центра, отличающихся нуклеофиль-ной способностью, по которым может идти реакция с XXIII. [2]
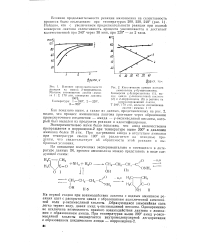 |
Влияние продолжительности реакции на выход 2-пирролидона Мольное соотношение лактон. аммиак 1, 2, 170 эти, конверсия лактона.| Кинетические кривые реакции. [3] |
Конверсия Y-бутиролактопа ( 1) выход амида у-оксимасляной кислоты ( 2) и 2-пирролидона ( 3) в расчете на т on Р РсагиРовавший лактон. [4]
При применении теоретического количества хлористого тионила выход амида снижается. [5]
При этом выделяется также вода, которая понижает выход амида. [6]
При разложении семикарбазона ( 3-фениламинобутанона разбавленной уксусной кислотой выход амида З - метил-пиразолин-1 - карбоновой кислоты достигает 28.7 % теоретического. [7]
И, действительно, в присутствии ледяной уксусной кислоты выход амида З - метилпиразолин-1 - кар-боновой кислоты намного выше, и продукт легко очищается перекристаллизацией из этилацетата. Еще лучшие результаты получаются при применении разбавленной уксусной кислоты. [8]
Установить соотношение изомеров в смеси нитрилов на основании данных о выходах соответствующих амидов не удается достаточно точно, так как, во-первых, для полного разделения амидов их необходимо хромато-графировать многократно, а при этом неизбежны значительные потери. Использованный в настоящей работе метод газо-жидкостной хроматографии позволил нам сравнительно точно установить соотношение изомеров в смесях нитрилов, полученных цианированием метил -, этил - и фенилферроцена. Данные табл. 1 свидетельствуют о том, что во всех исследованных случаях при цианировании получается значительно больше гомоаннулярных изомеров, чем гетероаннулярных. При переходе от ал-килферроценов к фенилферроцену относительное количество гетероанну-лярного изомера в смеси нитрилов значительно возрастает. [9]
Недостаток этого метода заключается в том, что реакция останавливается по достижении равновесия между аммониевой солью, амидом и водой, вследствие чего выхода амида часто бывают значительно ниже теоретических. Во избежание этого целесообразно пользоваться видоизменением способа, заключающимся в непрерывном удалении образующейся воды из сферы реакции. Нижеследующий пример дает представление об условиях применения этого способа. [10]
Аналогичным путем могут быть получены амиды и алкиламиды гомологов уксусной кислоты 4 - Недостаток этого метода заключается в том, что реакция останавливается по достижении равновесия между аммониевой солью, амидом и водой, вследствие чего выхода амида часто бывают значительно ниже теоретических. Во избежание этого целесообразно пользоваться видоизменением способа, заключающимся в непрерывном удалении образующейся воды из сферы реакции. Нижеследующий пример дает представление об условиях применения этого способа. [11]
Аналогичным путем могут быть получены амиды и алкиламиды гомологов уксусной кислоты Н - Недостаток этого метода заключается в том, что реакция останавливается по достижении равновесия между аммониевой солью, амидом и водой, вследствие чего выхода амида часто бывают значительно ниже теоретических. Во избежание этого целесообразно пользоваться видоизменением способа, заключающимся в непрерывном удалении образующейся воды из сферы реакции. Нижеследующий пример дает представление об условиях применения этого способа. [12]
Раствор выпаривается досуха, остаток ( амид тримеллитовой кислоты и следы амида ортофталевой кислоты) переносится в воронку, промывается 15 - 20 мл холодного ацетона или метиловым спиртом ( при этом удаляются следы амида ортофталевой кислоты), после чего вещество переносят на часовое стекло, высушивают до постоянного веса и определяют количество амида тримеллитовой кислоты. Выход амидов ортофталевой и тримеллитовой кислот по методу В. М. Родионова, но нашим экспериментальным данным, полученным с чистыми кислотами, колеблется в пределах 80 - 85 % от теории. Поэтому для выяснения истинного количества амидов тримеллитовой и ортофталевой кислот надо полученное во время опыта количество амидов умножить на 1 25, после чего сделать перс-счет на количество гримеллитовой и ортофталевой кислот. [13]
Содержание амида постоянно возрастает ( кривая 2) и достигает максимума ( 46 - 48 %) при 150 - 170 С. Дальнейшее повышение температуры реакции приводит к снижению выхода амида никотиновой кислоты за счет ускорения омыления его до никотиновой кислоты ( кривая 3), содержание которой при 210 С достигает 95 - 96 % от теоретически возможного. Приведенные на рис. 2 кинетические кривые процесса гидролиза З - цианпиридина вполне согласуются с литературными данными [1], где также отмечалось, что образование никотиновой кислоты идет через стадию образования амида никотиновой кислоты. [14]
Как правило, последовательность введения в реакционную смесь нитрила, хлористого водорода и воды не играет существенной роли. Однако в ряде случаев порядок добавления реагентов к реакционной смеси оказывает влияние на выход амидов. [15]
Страницы: 1 2