Ион - противоположный заряд
Cтраница 2
Каждый ион К или F окружен четырьмя ионами противоположного заряда и двумя молекулами воды, которые образуют почти октаэдричеекую структуру. [16]
Вместе с такими ионами к поверхности осадка притягиваются ионы противоположного заряда, которые сравнительно легко обмениваются на другие ионы при промывании осадка раствором электролита. [17]
 |
Кристаллическая шетка хлорида натрия. [18] |
Для устойчивости ионной решетки необходимо условие, чтобы ионы противоположного заряда соприкасались друг с другом. [19]
Подписываем под символами ионов левой части уравнения такие ионы противоположного заряда, которые образовали бы с исходными ионами растворимые сильные электролиты. [20]
 |
Кристаллические структуры некоторых ионных соединений. а - NaCl. б - CsCl. e - CaF2. [21] |
Это происходит благодаря электростатическому ( кулоновскому) притяжению ионов противоположных зарядов. [22]
Комплексообразование не ограничено, конечно, ассоциацией двух ионов противоположных зарядов. [23]
Простые ионы кобальта и железа могут присоединять не только ионы противоположного заряда, но и нейтральные молекулы, например Н2О, МН3 и др. При присоединении простыми ионами ионов противоположного заряда происходит изменение первоначальной зарядности простых ионов. [24]
 |
Диссоциация хлорида калия при 18 С. [25] |
В результате каждый ион окружается ионной атмосферой, состоящей из ионов противоположного заряда. Это уменьшает подвижность ионов. [26]
Вполне понятно, что ионный обмен можно использовать для разделения ионов противоположного заряда, которые участвуют в ионном обмене, и получить две отдельные соли. Раствор фторида хрома ( Ш), обработанный этилендиамином, образует ионы [ Cren2F2 ] красного цвета и [ CrenF4 ] - синего цвета. [27]
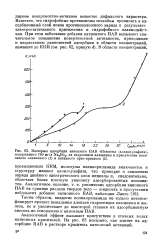 |
Изотермы адсорбции анионного ПАВ Новость ( алкилсульфата, содержащего 750 мг / л Na2SO4, на гидроокиси алюминия в присутствии катионного оливкового ( 1 и активного ярко-красного ( 2. [28] |
Известно, что гидрофобные противоионы способны проникать в адсорбционный слой ионов противоположного заряда в результате электростатического притяжения и гидрофобного взаимодействия. [29]
При добавлении электролита потенциал на поверхности частицы снижается за счет притягивания ионов противоположного заряда. Кроме того, разрушается диффузионный слой в результате дегидратации мицеллы. Взаимная нейтрализация заряда происходит при смешении двух золей с противоположно заряженными частицами. [30]
Страницы: 1 2 3 4