Ион - противоположный заряд
Cтраница 3
В настоящей статье под названием ионная пара имеются в виду пары ионов противоположного заряда, которые в некотором смысле действуют как единая частица и для которых достаточно допущения только электростатических сил связи. [31]
Выше указывалось, что многочисленные реакции изотопного обмена катализируются небольшими количествами ионов противоположного заряда - Многие из этих реакций использованы для изучения реакций комплексообразования ( см. гл. Однако для аналитических целей описано использование лишь одной из них. [32]
В случае отдачи электронов одними атомами и присоединения их другими атомами образуются ионы противоположных зарядов, которые затем притягиваются между собой и образуют молекулы. [33]
Наличие последующих максимумов на кривых распределения указывает на существование тенденции к чередованию ионов противоположного заряда. В табл. 32 приведены параметры первой и второй некоторых галогенидов щелочных металлов. [34]
Благодаря электростатическим силам притяжения или отталкивания вокруг каждого иона создается сгущенная атмосфера ионов противоположного заряда и разреженная атмосфера ионов, одноименных с ним. [35]
В твердом состоянии каждый ион обычно окружен четырьмя, шестью или восемью ионами противоположного заряда и поэтому кулоновская стабилизация значительно усиливается. [36]
В газах, жидкостях и кристаллах каждый ион стремится окружить себя наибольшим числом ионов противоположного заряда. Если представить ионы в виде несжимаемых сфер, то они располагаются в кристаллах друг около друга в определенном порядке, позволяющем занять минимально возможный объем с минимальной потенциальной энергией. [37]
При анализе большинства реальных образцов правильность определения содержания ионов снижается из-за присутствия некоторых ионов противоположного заряда. В этом и других случаях устранения мешающего влияния можно достичь за счет пропускания раствора образца через катионит в Н - форме. [38]
При внешнем соосаждении соосаждаемые ионы удерживаются на поверхности осадка в результате сил притяжения ионами противоположного заряда кристаллической решетки осадка. [39]
Действительно, каждый ион, находящийся внутри кристаллической решетки, взаимодействует с определенным числом ионов противоположного заряда ( например, с шестью в простой кубической решетке хлорида натрия), и таким образом его заряд нейтрализуется. Ион, находящийся на поверхности кристалла. Поэтому такие ионы особенно легко переходят в раствор. Чем меньше кристалл, тем большее относительное число его ионов находится на поверхности и тем больше поэтому его растворимость. Кристаллические частицы с неупорядоченными ионами также обнаруживают повышенную растворимость, так как такие ионы не входят в кристаллическую решетку и поэтому обладают повышенной энергией. Таким образом, со временем маленькие и неупорядоченные частицы осадка растворяются, а большие, более правильные и менее растворимые-растут. Растворимость осажденного вещества при этом понижается, пока не достигнет равновесной величины, соответствующей данной температуре. [40]
Действительно, каждый ион, находящийся внутри кристаллической решетки, взаимодействует с определенным числом ионов противоположного заряда ( например, с шестью в простой кубической решетке хлорида натрия), и таким образом его заряд нейтрализуется. Ион, находящийся на поверхности кристалла, имеет частично некомпенсированное электрическое поле, а те ионы, которые находятся на вершинах, в углах кристаллов, обладают особенно большим некомпенсированным полем и испытывают наиболее слабое притяжение со стороны решетки. Поэтому такие ионы особенно легко переходят в раствор. Чем меньше кристалл, тем большее относительное число его ионов находится на поверхности и тем больше поэтому его растворимость. Кристаллические частицы с неупорядоченными ионами также обнаруживают повышенную растворимость, так как такие ионы не входят в кристаллическую решетку и поэтому обладают повышенной энергией. Таким образом, со временем маленькие и неупорядоченные частицы осадка растворяются, а большие, более правильные и менее растворимые-растут. Растворимость осажденного вещества при этом понижается, пока не достигнет равновесной величины, соответствующей данной температуре. [41]
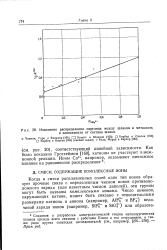 |
Изменение распределения марганца между шлаком и металлом. в зависимости от состава шлака. [42] |
Когда в смеси расплавленных солей один тип ионов образует прочные связи с определенным числом ионов противоположного заряда ( или известным числом диполей), эти группы могут быть названы комплексными ионами. [43]
Действительно, каждый ион, находящийся внутри кристаллической решетки, взаимодействует с определенным числом ионов противоположного заряда ( например, с шестью в простой кубической решетке хлорида натрия), и таким образом его - заряд: нейтрализуется. Ион, находящийся на поверхности кристалла, имеет частично некомпенсированное электрическое поле, а те ионы, которые находятся на вершинах, в углах кристаллов, обладают особенно большим некомпенсированным полем и испытывают наиболее слабое притяжение со стороны решетки. Поэтому такие ионы особенно легко переходят в раствор. Чем меньше кристалл, тем большее относительное число его ионов находится на поверхности и тем больше поэтому его растворимость. Кристаллические частицы с неупорядоченными ионами также обнаруживают повышенную растворимость, так как такие ионы не входят в кристаллическую решетку и поэтому обладают повышенной энергией. Таким образом, со временем маленькие и неупорядоченные частицы осадка растворяются, а большие, более правильные и менее растворимые-растут. Растворимость осажденного вещества при этом понижается, пока не достигнет равновесной величины, соответствующей данной температуре. [44]
 |
Зависимость скорости полимеризации от концентрации мономера. [45] |
Страницы: 1 2 3 4