Выход - метан
Cтраница 3
В таких случаях соотношение выходов метана и водорода может быть сравнимо по величине с результатами фотохимических и масс-спектроскопических исследований. При фотохимическом превращении газообразных алкилбензолов имеется небольшая вероятность передачи энергии, поглощенной кольцом, в боковую цепь. [31]
При замене н-гептана на толуол выход метана уменьшается до 60 - 65 % из-за присоединения метальных радикалов к толуолу. С увеличением отношения ТГФ: CH3TiCl3 Количество монодейтерометана уменьшается, что объясняется отрывом атома водорода не только от метильной группы толуола, но и от СН2 - групп в тетрагидрофуране. Применение полностью дейтерированного ТГФ и ( C2Ds) 2O подтверждает этот вывод. Избыток ТГФ не принимает, видимо, участия в реакции распада комплекса, так как константа скорости реакции при изменении отношения ТГФ: : CH3TiCl3 в 33 раза остается практически постоянной. [32]
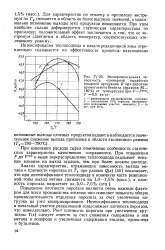 |
Экспериментальная зависимость суммарной выработки товарной продукции R при пиролизе лрямогонного бензина ( фракция 85 - 180 С от температуры при F FHOM. F 0 5 кг / кг. [33] |
Анализ характеристик, отражающих зависимость выхода метана и плотности пирогаза от Тв при разных Q ( x) [50 ] показывает, что при интенсификации теплоподвода в конечную часть реакционной зоны выход метана снижается на 1 0 - 1 5 % ( масс.), а плотность пирогаза возрастает на 5 0 - 7 0 % ( отн. [34]
 |
Диффузионный и кинетический режимы гидрирования окиси этилена. [35] |
По оси ординат отложены значения выхода метана V, по оси абсцисс - приведенная скорость водорода в барботажной колонне. Линия / соответствует температуре реакции 235 С, линия 2 - 261 С. При температуре 235 С реакция переходит в кинетическую область при wr; 0 1 м / с и дальнейшее увеличение расхода водорода слабо отражается на выходе метана. [36]
Здесь в циклическом режиме сильно увеличивался выход метана. [38]
При давлениях 8 0 МПа и выше выход метана начинает возрастать и принимать его ориентировочно нецелесообразно, тем более, что проведение прямых предварительных исследований процесса газификации при высоких давлениях представляет особые трудности. Для термодинамических расчетов по данной методике необходимо проведение большого ряда экспериментов с получением данных по выходу метена в газе и сажи в зависимости от различных начальных условий. Выполненные на пилотной установке эксперименты в основном подтверждают проведенные предварительные термодинамические расчеты, в том числе влияние водяного пара и температуры на равновесный состав газа. Вместе с тем опыты показали недостатки существующей методики при применении ее в области низких температур, когда существенно начинает расти выход сажи. [39]
Вода в топливе оказывает разное влияние на выход метана. В области высоких давлений ( 50 ата) и еще больших ( при Р 200 ата) увеличение содержания воды в топливе при низких температурах ( 1000 К) способствует образованию метана. Дальнейшее увеличение содержания воды, особенно при повышенных температурах ( 1300 - 1400 К), весьма заметно снижает содержание метана в газе. [40]
Результаты облучения некоторых углеводородов показали, что выход метана повышается с увеличением числа метальных групп в молекуле, в то время как количество образующегося водорода уменьшается. [41]
При фотолизе ацетона в газовой фазе отношение выхода метана, деленного на выход этана, пропорционально давлению ацетона. Предложите механизм, объясняющий этот результат. [42]
В растворах полистирола, натурального каучука и полиизопрена выход метана также снижается; авторы предполагают, что двойные связи винильного типа в боковых цепях более реакционноспособны по отношению к метальным радикалам, чем двойные связи в цепи. [43]
 |
Схема вычисления времени выхода неадсорбиру. [44] |
Описан также прямой метод [74] по определению времени выхода метана, как практически не адсорбируемого ( при достаточно высоких температурах колонки) газа. Однако этот метод не совсем точен, так как в некоторых случаях ( на активных адсорбентах) метан заметно адсорбируется. [45]
Страницы: 1 2 3 4 5
