Ион - йод
Cтраница 1
Ионы йода в кислой среде быстро восстанавливают ионы А4С4 - - - в АзОз - - - ( стр. [1]
 |
Возгонка йода ПаРЗМИ Й ДЭ окРашен в. [2] |
Ионы йода такого окрашивания не дают. Значит, крахмал является реактивом на йод. [3]
Окисляют ионы йода до йодата по Гроку [34], добавляя 2 капли раствора перманганата к кипящему раствору, и кипятят 5 мин. Если розовая окраска перманганата исчезнет, то добавляют его еще одну каплю. Через 2 мин добавляют по каплям раствор нитрита натрия до обесцвечивания и затем кипятят 5 мин. После охлаждения до комнатной температуры переносят раствор в мерную колбу на 50 мл и добавляют 3 0 мл раствора йодида калия и 4 0 мл раствора крахмала. Разбавляют раствор до метки, перемешивают и измеряют оптическую плотность через 30 мин при 575 ммк. [4]
Мешают ей и ионы йода, которые окисляются ионами Fe3 до свободного J2, придающего раствору красно-бурую окраску. Исследуемый раствор должен быть нейтральным. [5]
Практически при внесении иона йода в дозе до 100 мг / л биологическая очистка сточных вод, содержащих загрязнения, легко подвергающиеся биохимическому окислению, может проходить достаточно эффективно. [6]
В результате перескока электронов ионы йода, теряя электроны, переходят в молекулярный йод, а атом кислорода, получая эти электроны, переходит из атомарного в ионный и тут же, связываясь с ионами водорода, образует воду. [7]
Таким образом определяют концентрацию ионов йода. [8]
Это свидетельствует о том, что ионы йода сильнее взаимодействуют с твердой фазой, чем ионы серебра. [9]
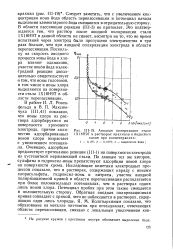 |
Анодная поляризация стали 1Х18Н9Т в растворах крахмала и йодистого. [10] |
Следует заметить, что с увеличением концентрации иона йода область перепассивации и потенциал начала выделения элементарного йода смещаются в отрицательную сторону. В области пассивации реакция ( II1 - 3) не протекает. Это подтверждается тем, что раствор после анодной поляризации стали 1Х18Н9Т в данной области не синеет, несмотря на то, что во время испытаний через электрод было пропущено электричества в три раза больше, чем при анодной поляризации электрода в области перепассивации. Поскольку на скорость анодного процесса ионы йода и хлора влияют одинаково, участие ионОв йода в электродной реакции дополнительно свидетельствует о том, что ионы галогенов, в том числе и ионы хлора выделяются на поверхности стали 1Х18Н9Т в области перепассивации. [11]
Шейн и Перон [3] описали метод определения иона йода с предварительным концентрированием на серебряном электроде, а Кемуля, Кублик и Тарашевска [4] применили для этой цели ртутный электрод. [12]
Примечание: Реакция проведена в присутствии большого избытка ионов йода. [13]
Зависимость максимального тока электрорастворения йодида ртути от концентрации ионов йода в растворе, по нашим данным [2], представляет собой прямую линию, отсекающую некоторый отрезок на оси абсцисс. [14]
Напишите формулы ацидокомплекса таллия, в котором аддендами служат ионы йода. [15]
Страницы: 1 2 3 4