Ион - кадмий
Cтраница 3
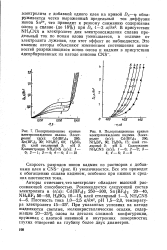 |
Поляризационные кривые электроосаждения кадмия. Электролит ( г / л. Cd ( BF4 2l 260. NH4BF4 60. НзВОз IS. клей сто-лярный 2. уН 2. Содержание. [31] |
Скорость разрядов ионов кадмия из растворов с добавками клея и CNS - ( рис, 8) увеличивается. Все это приводит к обогащению сплава кадмием, особенно при низких и средних плотностях тока. [32]
Поскольку восстановление ионов кадмия протекает быстро и обратимо, концентрация их в слое раствора, окружающем электрод, в любой момент определяется потенциалом кадмиевого электрода. При изменении потенциала мгновенно изменяется и концентрация ионов кадмия в приэлектродном слое в соответствии с уравнением Нернста, что приводит либо к выделению металлического кадмия на электроде, либо к растворению электрода. [33]
При взаимодействии ионов кадмия с нитропруссидом натрия образуется кристаллический осадок, хорошо поглощающий в области 365 - 280 нм. Цинк в отличие от кадмия не дает осадка с нитропруссидом. Каплю исследуемого раствора объемом 0 03 мл выпаривают почти досуха и вносят каплю 1 % - ного раствора нитропруссида натрия. Образуются кристаллы, которые при рассматривании под УФ-микроскопом окрашены в красный цвет. [34]
Равновесную концентрацию ионов кадмия в растворе рассчитывали, вычитая изначальной концентрации ионов кадмия то количество их, которое связано введенной щелочью. [35]
Возможно открытие ионов кадмия в виде фосфата кадмия. Для этого к капле исследуемого раствора объемом 0 03 мл прибавляют каплю раствора фосфата натрия и выпавший осадок рассматривают под ультрафиолетовым микроскопом. [36]
Трилонометрическос определение ионов кадмия. В колбу вносят 5 мл раствора, приливают 2 мл аммиачного буфера ( рН 10) п содержимое колбы разбавляют водой в 3 - 5 раз; добавляют небольшое количество индикатора эриохрома черного и титруют 0 05 М раствором трилона Б до перехода окраски раствора из красной ( красно-фиолетовой) в синюю. При добавлении последней капли рабочего раствора должен исчезнуть фиолетовый оттенок титруемого раствора. [37]
При реакциях ионов кадмия Cd2 с органическими реагентами состава Ar-NN-NH-Ar ( Ar и Аг - арильные радикалы), содержащими в качестве ФАГ диазоаминогруппу, образуются комплексы красного цвета. [38]
Мешают определению свинца ионы кадмия Cd2 и меди Си2 в концентрациях, превышающих концентрацию свинца в 100 раз. [39]
Осадок, содержащий ионы кадмия, растворяют в соляной кислоте, нейтрализуют и выполняют анализ, как описано. [40]
Для качественного определения ионов кадмия получают его комплекс с пиридином и иодидом калия. Выпадающий осадок состава [ Cc CsHsN ] Ь флуоресцирует сине-белым светом. [41]
Для измерения концентрации ионов кадмия, меди, мышьяка, теллура, свинца, сурьмы, хрома, цинка и других элементов, а также органических веществ в водных растворах. [42]
 |
Постояннотоковая подпрограмма восстановления кадмия ( II в 1 М растворе NaClO4 ( электрод сравнения Ag AgCl. [43] |
Процесс завершается диффузией ионов кадмия к электроду и металлического кадмия в ртутную каплю после перехода электронов через границу раздела ртуть - раствор. [44]
Для качественного определения ионов кадмия получают его комплекс с пиридином и иодидом калия. Выпадающий осадок состава [ Cd ( C5H5N) 2 ] l2 флуоресцирует сине-белым светом. [45]
Страницы: 1 2 3 4