Ион - ацетат
Cтраница 1
Ион ацетата Н3С - С00 - ( ас), подобно N03, может проявлять свойства как бидентатного, так и мостикового лиганда. [1]
Наряду с ионом ацетата, входящим в состав буферной смеси, образуется новая кислота, сопряженная с добавленным основанием. Важно, чтобы последнее было достаточно сильным, тогда равновесие будет полностью сдвинуто вправо. Получившаяся кислота должна быть достаточно слабой по сравнению с испытуемой. [2]
Определению не мешают ионы ацетата, алюминия, аммония, бромида, кальция, хлорида, трехвалентного хрома, кобальта, двухвалентной меди, бихромата, фторида, трехвалентного железа, двухвалентного свинца, двухвалентного марганца, молибдата, никеля, оксалата, перхлората, перманганата, калия, серебра, натрия, сульфата, ванадата и цинка. Мешают ионы силиката, арсената, арсенита, гер-маната и нитрита; их следует удалять перед первой экстракцией. Допустимо присутствие не более 200 мкг / мл нитрата и 20 мкг / мл вольфрамата. [3]
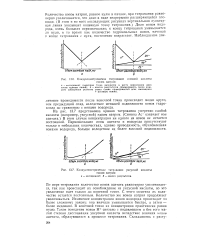 |
Коядукгометрическое титрование соляной кислоты едким натром.| Кондуктометрическое титрование уксусной кислоты. [4] |
По мере титрования количество ионов ацетата равномерно увеличивается, так как происходит их освобождение из уксусной кислоты, но это увеличение идет только до конечной точки. С этого момента их количество остается постоянным. Количество же ионов натрия продолжает увеличиваться. Изменение концентрации ионов водорода происходит по более сложному закону: она вначале уменьшается быстро, а затем - более медленно. В конечной точке их концентрация практически равна нулю. Такое поведение ионов Н связано с подавлением и без того малой степени диссоциации уксусной кислоты вследствие влияния ионов ацетата, образующихся в процессе титрования. [5]
В работе [113] было исследовано комплексообразование ура-нила с ионами ацетата ( Ас) путем совместного применения катио-нитов и анионитов. [6]
Второй тип разрыва связи в АТФ иллюстрирует реакция с ионом ацетата, в результате которой выделяется пирофосфат и монофосфо-риладенозинацетат. [7]
Авторы объясняют эти факты тем, что заряд на ионе ацетата затрудняет приближение ионов OD - или ND2 - и тем самым препятствует отрыву протона от углерода, ведущему к обмену. Сила отталкивания одноименных зарядов тем меньше, чем больше диэлектрическая постоянная среды. [8]
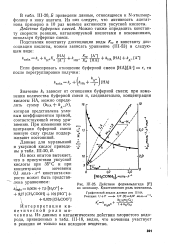
Как видно из рис. П-6, в случае комплексообразования иттрия с ионами ацетата [10 ] произведение у [ А ] первоначально возрастает с увеличением концентрации лиганда [ А ] ( за счет увеличения пропорциональной этому произведению величины амд), а затем начинает убывать вследствие образования последующих комплексных форм. [9]
Была выдвинута и другая теория, согласно которой активный анодный кислород окисляет ионы ацетата или уксусную кислоту в перекись ацетила ( СН3СО2) а, которая затем самопроизвольно разлагается, образуя этан и двуокись углерода. Продукты термического разложения перекиси ацетила и других перекисей, полученных химически, как показал опыт, оказались сходными с теми, которые образуются в результате электросинтеза Кольбе. Однако влияние вещества анода, а также катализаторов для разложения перекиси водорода и добавленных солей не может быть легко объяснено этой теорией. [10]
Количество образующейся уксусной кислоты равно количеству получающихся ионов гидроксила, а количество иона ацетата очень близко к количеству ацетата натрия ( соли) в растворе. [11]
К 2 мл нейтрального раствора ацетата ( 0 02 - 0 06 г иона ацетата) прибавляют 0 2 мл раствора хлорида окисного железа; появляется красно-бурое окрашивание, исчезающее при прибавлении разведенных минеральных кислот. [12]
Найдено, что замещение дейтерием вызывает уменьшение скорости реакции при катализе водой, ионом ацетата и ионом водорода; но уже отмечалось, что в реакции, сопровождающейся переносом двух протонов, это не исключает наличия предварительного равновесия. [13]
 |
Действие формальдегида [ F ] на мочевину. Кинетическая роль мочевины. [14] |
В табл. 111 - 20, Б приведены данные, относящиеся к N-этилмор-фолину и иону ацетата. Из них следует, что активность ацетат-иона примерно в 10 раз меньше активности уксусной кислоты. [15]
Страницы: 1 2 3 4