Ион - ацетат
Cтраница 2
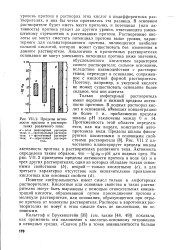 |
Пределы активности протона в растворителях различного типа. [16] |
Поэтому, например, в уксусной кислоте не может существовать основание более сильное, чем ион ацетата. [17]
Ацетат натрия, необходимый для протекания этой реакции, в случае хлорида палладия является источником ионов ацетата, участвующих во внутрисферной нуклеофильной атаке в процессе изомеризации я-комплекса в металлоорганическое соединение. [18]
Приведены сравнительные данные для н-и изобутана, полученные при применении А12О3 и бемита, модифицированного ионами ацетата или немодифицированного. [19]
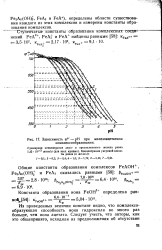 |
Зависимость q - рН при железоацетатном комплексообразовании. [20] |
Из приведенных величин констант видно, что комплексо-рбразующая способность иона гидроксила во много раз больше, чем иона ацетата. [21]
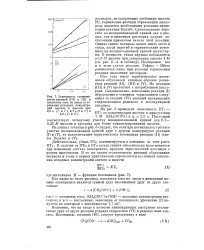 |
Зависимость селективности реакций ( III и ( II и плотности тока на аноде от отношения исходных концентраций ацетата и щелочи при 2 5 е ( 1 и 1, 2 7 в ( 2 и 2 и 3 0 в ( 3 и 3. [22] |
Возможно, что на аноде в качестве лимитирующих выступают независимые друг от друга реакции разряда гидроксила ( VI) и разряда иона ацетата. [23]
Жидкий аммиак, в отличие от воды, является дифференцирующим растворителем для значительно более сильных оснований; основания в воде более сильные, чем ион ацетата, в ледяной уксусной кислоте приравниваются к нему. [24]
Пат-зак и ЗакиМ изучили полярографическое поведение циркония на капельном ртутном электроде в присутствии красителя солохромфиолето - BoroRS и разработали метод определения циркония в присутствии тория, маскируя торий ионами ацетата. Комплекс циркония с солохромфиолето-вым RS дает четкие волны в интервале значений рН 2 - 4 при потенциалах в области ( - 0 3) - ( - 0 5) В. [25]
Оба способа основаны на том, что монофункциональная иминодиуксусная смола образует с ионами металлов из ацетатного буфера более устойчивые комплексные формы, чем формы, соответствующие величине DpH, поскольку дополнительно координируются ионы ацетата. Кислоты, используемые для элюирования, могут частично разлагать эти устойчивые комплексные формы. [26]
О расщепляющей способности три-фторуксусного ангидрида упоминалось выше; Р1, Р2 - диаденозин-5 - пирофосфат также расщепляется уксусным ангидридом ( вследствие аддитивных свойств карбонильной группы), но устойчив к нуклео-фильной атаке ионом ацетата, поскольку это означало бы освобождение менее устойчивого аниона. [27]
В результате изучения электролиза ацетатов в водном растворе эти исследователи пришли к выводу, что перекись водорода, первоначально образующаяся на аноде из гидроксильных радикалов, или сами гидроксильные радикалы до объединения их в пары, реагируют с ионами ацетата, давая ацетатные радикалы. [28]
Хотя электродная функция относительно анионов, имеющих малое сродство к протонам, например перхлоратов или бензолсульфонатов, мало зависит от рН ( в пределах 2 - 10), зависимость потенциала от концентрации анионов, проявляющих основные свойства, например ионов ацетата или бензоата, меняется при снижении рН до значений, обусловливающих переход части анионов в кислоту. [29]
Под действием электрического тока ионы натрия перемещаются к катоду, захватывают электроны и образуют едкий натр и водород. Ионы ацетата перемещаются к аноду, отдают свой заряд, вероятно с образованием неустойчивого ацетатного свободного радикала с неспаренным электроном у кислорода. От этого радикала тотчас же отщепляется двуокись углерода и образуется неустойчивый метальный радикал с неспаренным электроном. [30]
Страницы: 1 2 3 4